三、植物活性成分的分离与精制
(一)根据化合物溶解度不同进行分离
1.结晶、重结晶和分步结晶法
鉴定植物化学成分,研究其化学结构,必须首先将植物成分制备成单体纯品。在常温下,物质本身性质是液体的化合物,可分别用分馏法或层析法进行分离精制。一般的说,植物化学成分在常温下多半是固体的物质,都具有结晶化的通性,可以根据溶解度的不同用结晶法来达到分离精制的目的。研究植物化学成分时,一旦获得结晶,就能有效地进一步精制成为单体纯品。纯化合物的结晶有一定的熔点和结晶学的特征,有利于鉴定。如果鉴定的物质不是单体纯品,不但不能得出正确的结论,还会造成工作上的浪费。因此,求得结晶并制备成单体纯品,就成为鉴定植物成分、研究其分子结构重要的一步。
(1)杂质的除去:植物样品经过提取所得到的成分,大多仍然含有杂质,或者是混合成分。有时即使有少量或微量杂质存在,也能阻碍或延缓结晶的形成。所以在制备结晶时,必须注意杂质的干扰,应力求尽可能除去。有时可选用溶剂溶出杂质,或只溶出所需要的成分。有时可用少量活性炭等进行脱色处理,以除去有色杂质。有时可通过氧化铝,硅胶或硅藻土短柱处理后,再进行制备结晶。但应用吸附剂除去杂质时,要注意所需要的成分也可能被吸附而损失。此外,层析法更是分离制备单体纯品所常用的有效方法。
如果一再处理仍未能使近于纯品的成分结晶化,则可先制备其晶态的衍生物,再回收原物,可望得到结晶。例如游离生物碱可制备各种生物碱盐类,羟基化合物可转变成乙酰化物,羰基化合物可制备成苯腙衍生物结晶。如美登碱在原料中含量少,且反复分离精制难以得到结晶,但制备成3—溴丙基美登碱结晶后,再经水解除去溴丙基,美登碱就能制备成为结晶。
(2)溶剂的选择:制备结晶,要注意选择适宜的溶剂和应用适量的溶剂。适宜的溶剂,最好是在冷时对所需要的成分溶解度小,而热时溶解度大。溶剂的沸点亦不宜太高,一般常用甲醇、丙酮、氯仿、乙醇、乙酸乙酯等,但有些化合物在一般溶剂中不易形成结晶,而在某些溶剂中则易于形成结晶。例如葛根素、逆没食子酸(e11agicacid)在冰醋酸中易形成结晶,大黄素(emodin)在吡啶中易于结晶,萱草毒素(hemerocallin)在N,N-二甲基甲酰胺(DMF)中易得到结晶,而穿心莲亚硫酸氢钠加成物在丙酮-水中较易得到结晶。又如蝙蝠葛碱通常为无定形粉末,但能和氯仿或乙醚形成加成物结晶。
(3)结晶溶液的制备:制备结晶的溶液,需要成为过饱和的溶液。一般是应用适量的溶剂在加温的情况下,将化合物溶解再放置冷处。如果在室温中可以析出结晶,就不一定放置于冰箱中,以免伴随结晶析出更多的杂质。
“新生态”的物质即新游离的物质或无定形的粉末状物质,远较晶体物质的溶解度大,易于形成过饱和溶液。一般经过精制的化合物,在蒸去溶剂抽松为无定形粉末时就是如此,有时只要加入少量溶剂,往往立即可以溶解,稍稍放置即能析出结晶。例如长春花总弱碱部分抽松后加入1.5倍量的甲醇溶解,放置后很快析出长春碱结晶。又如蝙蝠葛碱在乙醚中很难溶解,但当其盐的水溶液用氨液碱化,并立即用乙醚萃取,所得的乙醚溶液,放置后即可析出蝙蝠葛碱的乙醚加成物结晶。
制备结晶溶液,除选用单一溶剂外,也常采用混合溶剂。一般是先将化合物溶于易溶的溶剂中,再在室温下滴加适量的难溶的溶剂,直至溶液微呈浑浊,并将此溶液微微加温,使溶液完全澄清后放置。例如,α-细辛醚重结晶时,可先溶于乙醇,再滴加适量水,即可析出很好的结晶。又如自虎杖中提取水溶性的虎杖甙(polydatln)时,在已精制饱和的水溶液上添加一层乙醚放置,既有利于溶出其共存的脂溶性杂质,又可降低水的极性,促使虎杖甙的结晶化。自秦皮中提取七叶甙(秦皮甲素),也可运用这样的办法。
结晶过程中,一般是溶液浓度高,降温快,析出结晶的速度也快些。但是其结晶的颗粒较小,杂质也可能多些。有时自溶液中析出的速度太快,超过化合物晶核的形成和分子定向排列的速度,往往只能得到无定形粉末。有时溶液太浓,黏度大反而不易结晶化。如果溶液浓度适当,温度慢慢降低,有可能析出结晶较大而纯度较高的结晶。有的化合物其结晶的形成需要较长的时间,例如铃兰毒甙等,有时需放置数天或更长的时间。
(4)制备结晶操作:制备结晶除应注意以上各点外,在放置过程中,最好先塞紧瓶塞,避免液面先出现结晶,而致结晶纯度较低。如果放置一段时间后没有结晶析出,可以加入极微量的种晶,即同种化合物结晶的微小颗粒。加种晶是诱导晶核形成常用而有效的手段。一般的说,结晶化过程是有高度选择性的,当加入同种分子或离子,结晶多会立即长大。而且溶液中如果是光学异构体的混合物,还可依种晶性质优先析出其同种光学异构体。没有种晶时,可用玻璃棒蘸过饱和溶液一滴,在空气中任溶剂挥散,再用以摩擦容器内壁溶液边缘处,以诱导结晶的形成。如仍无结晶析出,可打开瓶塞任溶液逐步挥散,慢慢析晶。或另选适当溶剂处理,或再精制一次,尽可能除尽杂质后进行结晶操作。
(5)重结晶及分步结晶:在制备结晶时,最好在形成一批结晶后,立即倾出上层溶液,然后再放置以得到第二批结晶。晶态物质可以用溶剂溶解再次结晶精制。这种方法称为重结晶法。结晶经重结晶后所得各部分母液,再经处理又可分别得到第二批、第三批结晶。这种方法则称为分步结晶法或分级结晶法。晶态物质在一再结晶过程中,结晶的析出总是越来越快,纯度也越来越高。分步结晶法各部分所得结晶,其纯度往往有较大的差异,但常可获得一种以上的结晶成分,在未加检查前不要贸然混在一起。
(6)结晶纯度的判定:化合物的结晶都有一定的结晶形状、色泽、熔点和熔距,可以作为鉴定的初步依据。这是非结晶物质所没有的物理性质。化合物结晶的形状和熔点往往因所用溶剂不同而有差异。原托品碱在氯仿中形成棱柱状结晶,熔点207℃;在丙酮中则形成半球状结晶,熔点203℃;在氯仿和丙酮混合溶剂中则形成以上两种晶形的结晶。又如N—氧化苦参碱,在无水丙酮中得到的结晶熔点208℃,在稀丙酮(含水)析出的结晶为162~164℃。所以文献中常在化合物的晶形、熔点之后注明所用溶剂。一般单体纯化合物结晶的熔距较窄,有时要求在0.5℃左右,如果熔距较长则表示化合物不纯。但有些例外情况,特别是有些化合物的分解点不易看得清楚。也有的化合物熔点一致,熔距较窄,但不是单体。一些立体异构体和结构非常类似的混合物,常有这样的现象。还有些化合物具有双熔点的特性,即在某一温度已经全部融熔,当温度继续上升时又固化,再升温至一定温度又熔化或分解。如防己诺林碱在176℃时熔化,至200℃时又固化,再在242℃时分解。植物成分经过同一溶剂进行三次重结晶,其晶形及熔点一致,同时在薄层层析或纸层层析法经数种不同展开剂系统检定,也为一个斑点者,一般可以认为是一个单体化合物。但应注意,有的化合物在一般层析条件下,虽然只呈现一个斑点,但并不一定是单体成分。例如鹿含草中主成分为高熊果甙(homoarbutin),异高熊果甙(isobomoarbutin),极难用一般方法分离,经反复结晶后,在纸层及聚酰胺薄层上都只有一个斑点。易误认为单一成分,但测其熔点在115~125℃,熔距很长。经制备其甲醚后,再经纸层层析检定,可以出现两个斑点,异高熊果甙的Rf值大于高熊果甙。又如水菖蒲根茎挥发油中的α-细辛醚和β-细辛醚,在一般薄层上均为一个斑点,前者为结晶,熔点63℃,后者为液体,沸点296℃,用硝酸银薄层或气相层析很容易区分。有时个别化合物(如氨基酸)可能部分地与层析纸或薄层上的微量金属离子(如Cu2+)、酸或碱形成络合物、盐或分解而产生复斑。因此,判定结晶纯度时,要依据具体情况加以分析。此外,高压液相色谱、气相层析、紫外光谱等,均有助于检识结晶样品的纯度。
2.沉淀法
沉淀法是在植物提取液中加入某些试剂使产生沉淀,以获得有效成分或除去杂质的方法。
(1)铅盐沉淀法:铅盐沉淀法为分离某些中草药成分的经典方法之一。由于醋酸铅及碱式醋酸铅在水及醇溶液中,能与多种植物成分生成难溶的铅盐或络盐沉淀,故可利用这种性质使有效成分与杂质分离。通常将植物的水或醇提取液先加入醋酸铅浓溶液,静置后滤出沉淀,并将沉淀洗液并入滤液,于滤液中加碱式醋酸铅饱和溶液至不发生沉淀为止。这样就可得到醋酸铅沉淀物、碱式醋酸铅沉淀物及母液三部分。然后将铅盐沉淀悬浮于新溶剂中,通以硫化氢气体,使分解并转化为不溶性硫化铅而沉淀。含铅盐母液亦须先如法脱铅处理,再浓缩精制。硫化氢脱铅比较彻底,但溶液中可能存有多余的硫化氢,必须先通入空气或二氧化碳让气泡带出多余的硫化氢气体,以免在处理溶液时参与化学反应。新生态的硫化铅多为胶体沉淀,能吸附提取液中的有效成分,要注意用溶剂处理收回。脱铅方法,也可用硫酸、磷酸、硫酸钠、磷酸钠等除铅,但硫酸铅、磷酸铅在水中仍有一定的溶解度,除铅不彻底。用阳离子交换树脂脱铅快而彻底,但要注意提取液中某些有效成分也可能被交换上去,同时脱铅树脂再生也较困难。还应注意脱铅后溶液酸度增加,有时需中和后再处理溶液,有时可用新制备的氢氧化铅、氢氧化铝、氢氧化铜或炭化铅、明矾等代替醋酸铅、碱式醋酸铅。例如在黄芩水煎液中加入明矾溶液,黄芩甙就与铝盐结合生成难溶于水的络化物而与杂质分离,这种络化物经用水洗净就可直接使用。
(2)试剂沉淀法:例如在生物碱盐的溶液中,加入某些生物碱沉淀试剂,则生物碱生成不溶性复盐而析出。水溶性生物碱难以用萃取法提取分出,常加入雷氏铵盐使生成生物碱雷氏盐沉淀析出。又如橙皮甙,芦丁、黄芩甙、甘草皂甙均易溶于碱性溶液,当加入酸后可使之沉淀析出。某些蛋白质溶液,可以变更溶液的pH值,利用其在等电点时溶解度最小的性质而使之沉淀析出。
此外,还可以用明胶、蛋白溶液沉淀鞣质;胆甾醇也常用以沉淀洋地黄皂甙等。可根据植物有效成分和杂质的性质,适当选用。
(3)盐析法:盐析法是在中草药的水提液中,加入无机盐至一定浓度,或达到饱和状态,可使某些成分在水中的溶解度降低沉淀析出,而与水溶性大的杂质分离。常用作盐析的无机盐有氯化钠、硫酸钠、硫酸镁、硫酸铵等。例如三七的水提取液中加硫酸镁至饱和状态,三七皂甙乙即可沉淀析出;自黄藤中提取掌叶防己碱,自三棵针中提取小檗碱在生产上都是用氯化钠或硫酸铵盐析制备。有些成分如原白头翁素、麻黄碱、苦参碱等水溶性较大,在提取时,亦往往先在水提取液中加入一定量的食盐,再用有机溶剂萃取。
(二)根据有机化合物在两相溶剂中的分配比不同进行分离
1.溶剂分离法
一般是将植物的总提取物,选用3、4种不同极性的溶剂,由低级性到高级性分步进行提取分离。水浸膏或乙醇浸膏常为胶状物,难以均匀分散在低级性溶剂中故不能提取完全,可拌入适量惰性填充剂,如硅藻土或纤维粉等,然后低温或自然干燥,粉碎后,再以选用溶剂依次提取。使总提取物中各组成成分,依其在不同极性溶剂中溶解度的差异而得到分离。例如粉防己乙醇浸膏,碱化后可利用乙醚溶出脂溶性生物碱,再以冷苯处理溶出粉防己碱,与其结构类似的防己诺林碱比前者少一甲基而有一酚羟基,不溶于冷苯而得以分离。利用植物化学成分,在不同极性溶剂中的溶解度进行分离纯化,是最常用的方法。
2.两相溶剂萃取法
(1)萃取法:两相溶剂提取又简称萃取法,是利用混合物中各成分在两种互不相溶的溶剂中分配系数的不同而达到分离的方法。萃取时如果各成分在两相溶剂中分配系数相差越大,则分离效率越高。如果在水提取液中的有效成分是亲脂性的物质,一般多用亲脂性有机溶剂,如苯、氯仿或乙醚进行两相不取;如果有效成分是偏于亲水性的物质,在亲脂性溶剂小难溶解,就需要改用弱亲脂性的溶剂,例如乙酸乙酯、丁醇等。还可以在氯仿、乙醚中加入适量乙醇或甲醇以增大其亲水性。提取黄酮类成分时,多用乙酸乙酯和水的两相萃取。提取亲水性强的皂甙则多选用正丁醇、异戊醇和水作两相萃取。不过,一般有机溶剂亲水性越大,与水作两相萃取的效果就越不好,因为能使较多的亲水性杂质伴随而出,对有效成分进一步精制影响很大。
两相溶剂萃取在操作中还要注意以下几点:①先用小试管猛烈振摇约1min,观察萃取后两液层分层现象。如果容易产生乳化,大量提取时要避免猛烈振摇,可延长萃取时间。如碰到乳化现象,可将乳化层分出,再用新溶剂萃取;或将乳化层抽滤;或将乳化层稍稍加热;或较长时间放置并不时旋转,令其自然分层。乳化现象较严重时,可以采用二相溶剂逆流连续萃取装置。②水提取液的浓度最好在比重1.1~1.2之间,过稀则溶剂用量太大,影响操作。③溶剂与水溶液应保持一定量的比例,第一次萃取时,溶剂要多一些,一般为水提取液的1/3,以后的用量可以少一些,一般1/4~1/6。④一般萃取3~4次即可。但亲水性较大的成分不易转入有机溶剂层时,须增加萃取次数,或改变萃取溶剂。
液-液萃取中常遇到乳化问题,影响提取分离操作的进行,至今还没有一个比较成熟的乳状液理论。一般形成乳状液要有不互溶的两相溶剂、外力、界面活性物质(一些植物天然成分如皂甙、蛋白质、多种植物胶质等,都是表面活性物质)等几个条件。植物成分分离时,一般都具备这三个条件,因而萃取过程的乳化问题比较突出,防止萃取过程发生乳化和破乳是液-液萃取的重要问题。
关于乳状液的形成和稳定性有多种学说,如界面张力学说、界面吸附膜学说、定向锲学说、复合膜学说、稳定性的电学理论(双电层理论)、固体的稳定作用等。概括起来,乳状液液滴界面上由于表面活性物质或固体粉粒的存在,而形成了一层牢固的带有电荷的膜(固体粉粒膜不带电荷),因而阻碍液滴的聚结分层。乳状液虽有一定的稳定性,但乳状液具有高的分散度、表面积大、表面自由能高,是一个热力学不稳定体系,它有聚结分层、降低体系能量的趋势。

图2-1 用氯仿从川楝皮水浸液中萃取川楝素装置示意图1.萃取管;2.填料层;3.水浸液高位容器;4.氯仿贮存器;5.旋塞
破乳就是利用其不稳定性,削弱和破坏其稳定性,使乳状液破坏。破乳的原理主要是破坏它的膜和双电层,按其方法分为:①顶替法:加入表面活性更强的物质,把原来的界面活性剂顶替出来,常用低级醇,如戊醇,其界面活性强,但碳链短,不能形成牢固的膜而使乳状液破坏。②变型法:针对乳状液类型和界面活性剂类型,加入相反的界面活性剂,促使乳状液转型,在未完全转型的过程中将其破坏。如阳离子表面活性剂溴代十五烷吡啶(P.P.B)用于破坏W/O型乳状液,阴离子型如十二烷基磺酸钠,用于破坏O/W型乳状液。③反应法:如已知乳化剂种类,可加入能与之反应的试剂,使之破坏、沉淀。如皂类乳化剂加入酸;钠皂加入钙盐等。对离子型乳化剂,因其稳定性主要是其双电层维持,可加入高价电解质,破坏其双电层和表面电荷,使乳状液破坏。④物理法;加热是常使用的方法。加热可使布朗运动加快,增加液滴碰撞几率,加快絮凝速度;由于液体黏度与液体的绝对温度的倒数成指数关系,即温度升高不多而黏度降低很大,界面膜易破裂。⑤离心法:主要利用比重差异促使分层。离心和抽滤中不可忽视一个个液滴压在一起的重力效应,它足以克服双电层的斥力,促进凝聚(P.贝歇尔,1978)。
(2)逆流连续萃取法:是一种连续的两相溶剂萃取法。其装置可具有一根、数根或更多的萃取管。管内用小瓷圈或小的不锈钢丝圈填充,以增加两相溶剂萃取时的接触面。例如用氯仿从川楝树皮的水浸液中萃取川楝素(toosendanin),其装置如图2-1。将氯仿盛于萃取管内,而比重小于氯仿的水提取浓缩液贮于高位容器内,开启活塞,则水浸液在高位压力下流入萃取管,遇瓷团撞击而分散成细粒,使与氯仿接触面增大,萃取就比较完全。如果一种植物的水浸液需要用比水轻的苯、乙酸乙酯等进行萃取,则需将水提浓缩液装在萃取管内,而苯、乙酸乙酯贮于高位容器内。萃取是否完全,可取样品用薄层层析、纸层析及显色反应或沉淀反应进行检查。

图2-2 液滴逆流分配法的移动相与固定相示意图A.流动相;B.固定相
(3)逆流分配法(CounterCurrentDistribution,CCD):逆流分配法又称逆流分溶法、逆流分布法或反流分布法。逆流分配法与两相溶剂逆流萃取法原理一致,但加样量一定,并不断在一定容量的两相溶剂中,经多次移位萃取分配而达到混合物的分离。本法所采用的逆流分布仪是由若干乃至数百只管子组成。若无此仪器,小量萃取时可用分液漏斗代替。预先选择对混合物分离效果较好,即分配系数差异大的两种不相混溶的溶剂。并参考分配层析的行为分析推断和选用溶剂系统,通过试验测知要经多少次的萃取移位而达到真正的分离。
(4)液滴逆流分配法(DropletCounterCurrentChroma-tography,DCCC):液滴逆流分配法又称液滴逆流层析法。为近年来在逆流分配法基础上改进的两相溶剂萃取法。目前应用的仪器是将内径为2.4mm,高60cm,分配萃取管25管接连一板,共装12板,合计300管的连续分配萃取管。对溶剂系统的选择基本同逆流分配法,但要求能在短时间内分离成两相,并可生成有效的液滴(见图2-2,2-3)。由于移动相形成液滴,在细的分配萃取管中与固定相有效地接触、摩擦不断形成新的表面,促进溶质在两相溶剂中的分配,故其分离效果往往比逆流分配法好。且不会产生乳化现象;用氮气压驱动移动相,被分离物质不会因遇大气中氧气而氧化。本法必须选用能生成液滴的溶剂系统,且对高分子化合物的分离效果较差,处理样品量小(1g以下),并要有一定设备。应用液滴逆流分配法能有效地分离多种微量成分如柴胡皂甙原小檗碱型季铵碱等。
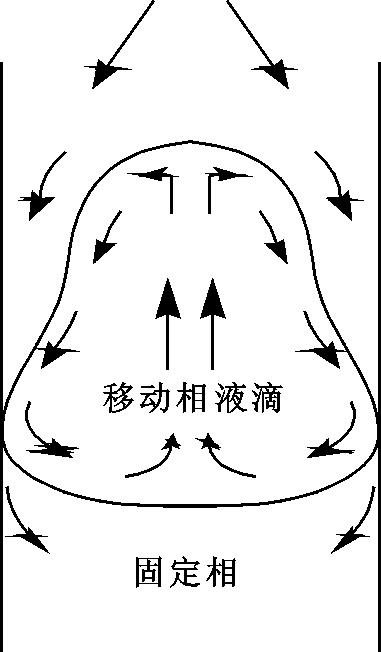
图2-3 移动相液滴与固定相之间分配示意图
(三)根据有机化合物的吸附能力不同进行分离
吸附层析法(AdsorptionChromatography)的应用与发展,对于各类植物化学成分的分离精制工作起到很大的推动作用。吸附柱层析和薄层层析是主要的吸附层析手段。
1.吸附柱层析
(1)吸附剂、溶剂与被分离物性质的关系:液—固吸附层析是运用较多的一种方法,特别适用于很多中等分子量的样品(分子虽小于1000的低挥发性样品)的分离,尤其是脂溶性成分。一般不适用于高分子量样品如蛋白质、多糖或离子型亲水性化合物等的分离。吸附层析的分离效果,决定于吸附剂、溶剂和被分离化合物的性质这三个因素。常用的吸附剂主要有硅胶、氧化铝、聚酰胺、活性炭、硅酸镁、硅藻土等。
硅胶:层析用硅胶为一多孔性物质,可用通式SiO2XH2O来表示。分子中具有硅氧烷(-Si-O-Si-)的交链结构,同时在颗粒表面又有很多硅醇基(SiOH)结构。硅胶吸附作用的强弱与硅醇基的含量多少有关。硅醇基能够通过氢键的形成而吸附水分,因此硅胶的吸附力随吸着的水分增加而降低。若吸水量超过17%,吸附力极弱,不能用作为吸附剂,但可作为分配层析中的支持剂。所以使用前,应对硅胶加热至100~110℃活化0.5~1h。
氧化铝:氧化铝可能带有碱性(因其中可混有碳酸钠等成分),对于分离一些碱性成分,如生物碱类的分离颇为理想。但是碱性氧化铝不适用于醛、酮、酯、内酯等类型的化合物分离。因为有时碱性氧化铝可与上述成分发生次级反应,如异构化、氧化、消除反应等。除去氧化铝中的碱性杂质可用水洗至中性,称为中性氧化铝。中性氧化铝仍属于碱性吸附剂的范畴,不适用于酸性成分的分离。用稀硝酸或稀盐酸处理氧化铝,不仅可中和氧化铝中含有的碱性杂质,并可使氧化铝颗粒表面带有NO3-或Cl-的阴离子,从而具有离子交换剂的性质,适合于酸性成分的层析,这种氧化铝称为酸性氧化铝。
供层析用的氧化铝,用于柱层析的,其粒度要求在100~160目之间。粒度大于100目,分离效果差;小于160目,溶液流速太慢,易使谱带扩散。样品与氧化铝的用量比,一般在1∶20~50之间,层析柱的内径与柱长比例在1∶10~20之间。
活性炭:是使用较多的一种非极性吸附剂。一般需要先用稀盐酸洗涤,其次用乙醇洗,再以水洗净,于80℃干燥后即可供层析用。层析用的活性炭,最好选用颗粒活性炭,若为活性炭细粉,则需加入适量硅藻土作为助滤剂一并装柱,以免流速太慢。
活性炭主要用于分离水溶性成分,如氨基酸、糖类及某些甙。活性炭的吸附作用,在水溶液中最强,在有机溶剂中则较弱。故水的洗脱能力最弱,而有机溶剂则较强。例如以醇-水进行洗脱时,则随乙醇浓度的递增而洗脱力增加。
活性炭对芳香族化合物的吸附力大于脂肪族化合物;对大分子化合物的吸附力大于小分子化合物。利用这些吸附性的差别,可将水溶性芳香族物质与脂肪族物质分开,单糖与多糖分开,氨基酸与多肽分开。
(2)溶剂:层析过程中溶剂的选择,对组分分离关系极大。在柱层析时所用的溶剂(单一溶剂或混合溶剂)习惯上称洗脱剂,用于薄层或纸层析时常称展开剂。
洗脱剂的选择,须根据被分离物质与所选用的吸附剂性质这两者结合起来加以考虑。
在用极性吸附剂进行层析时,当被分离物质为弱极性物质,一般选用弱极性溶剂为洗脱剂;被分离物质为强极性成分,则须选用极性溶剂为洗脱剂。如果对其一极性物质用吸附性较弱的吸附剂(加以硅藻土或滑石粉代替硅胶),则洗脱剂的极性亦须相应降低。
在柱层操作时,被分离样品在加样时可采用干法,亦可选一适宜的溶剂将样品溶解后加入。溶解样品的溶剂应选择极性较小的,以便被分离的成分可以被吸附。然后渐增大溶剂的极性。这种极性的增大是一个十分缓慢的过程,称为“梯度洗脱”,使吸附在层析柱上的各个成分逐个被洗脱。如果极性增大过快(梯度太大),就不能获得满意的分离。溶剂的洗脱能力,有时可以用溶剂的介电常数来表示。介电常数高,洗脱能力就大。吸附柱层析常用的混合洗脱溶剂(按极性递增的顺序)主要有:
石油醚-苯→苯-乙醚→苯-乙酸乙酯→氯仿-乙醚→氯仿-乙酸乙酯→氯仿-丙酮→氯仿-甲醇→丙酮-水→甲醇-水
(3)被分离物质的性质:被分离的物质与吸附剂、洗脱剂共同构成吸附层析中的三个要素,彼此紧密相连。在指定的吸附剂与洗脱剂的条件下,各个成分的分离情况,直接与被分离物质的结构与性质有关。对极性吸附剂而言,成分的极性大,吸附性强。一般按下列顺序增强其吸附性。
-CH2-CH2-,-CH=CH-,-OCH3,-COOR-,>C=O,-CHO,-SH,-NH2,-OH,-COOH
当然,植物成分的整体分子观是重要的,例如极性基团的数目愈多,被吸附的性能就会更大些,在同系物中碳原子数目少些,被吸附也会强些。总之,只要两个成分在结构上存在差别,就有可能分离,关键在于条件的选择。要根据被分离物质的性质(例如极性大小),吸附剂的吸附强度与溶剂的性质这三者的相互关系来考虑。
2.薄层层析(thinlayerchromatography,TLC)
薄层层析是一种简便、快速、微量的层析方法。一般将柱层析用的吸附剂撒布到平面如玻璃片上,形成一薄层进行层析时,即称薄层层析。其原理与柱层析基本相似。
(1)薄层层析的特点:薄层层析在应用与操作方面的特点与柱层析的比较见表2-1。
(2)吸附剂的选择:薄层层析用的吸附剂与其选择原则和柱层析相同。主要区别在于薄层层析要求吸附剂(支持剂)的粒度更细,一般应小于250目,并要求粒度均匀。用于薄层层析的吸附剂或顶制薄层一般活度不宜过高,以Ⅱ~Ⅲ级为宜。而展开距离则随薄层的粒度粗细而定,薄层粒度越细,展开距离相应缩短,一股不超过10cm,否则可引起色谱扩散影响分离效果。
表2-1 柱层析与薄层层析的比较表

(3)展开剂的选择:薄层层析,当吸附剂活度为一定值时(如Ⅱ或Ⅲ级),对多组分的样品能否获得满意的分离,决定于展开剂的选择。植物化学成分在脂溶性成分中,大致可按其极性不同而分为无极性、弱极性、中极性与强极性。但在实际工作中,经常需要利用溶剂的极性大小,对展开剂的极性予以调整。
(4)特殊薄层,针对某些性质特殊的化合物的分离与检出,有时需采用一些特殊薄层。例如,荧光薄层、络合薄层、酸碱薄层和pH缓冲薄层。
①荧光薄层:有些化合物本身无色,在紫外灯下也不显荧光,又无适当的显色剂时,则可在吸附剂中加入荧光物质制成荧光薄层进行层析。展层后置于紫外光下照射,薄层板本身显荧光,而样品斑点处不显荧光,即可检出样品的层析位置。常用的荧光物质多为无机物。其一是在254nm紫外光激发下显出荧光的,如锰激活的硅酸锌(Zn2SiO4:Mn)。另一种为在365nm紫外光激发下发出荧光的,如银激化的硫化锌硫化镉(ZnS·CdS:Ag)。
②络合薄层:常用的有硝酸银薄层,用来分离碳原子数相等,而其中C=C双键数目不等的一系列化合物,如不饱和醇、酸等。其主要机理是由于C=C键能与硝酸银形成络合物,而饱和的C—C键则不与硝酸银结合。因此在硝酸银薄层上,化合物可由于饱和程度不同而获得分离。层析时饱和化合物由于吸附最弱而Rf值高,含一个双键的较含两个双键的Rf值高,含一个三键的较含一个双键的Rf值高。此外,在一个双键化合物中,顺式的与硝酸银络合较反式的易于进行。因此,还可用来分激顺反异构体。
③酸碱薄层和pH缓冲薄层:为了改变吸附剂原来的酸碱性,可在铺制薄层时采用稀酸或稀碱以代替水调制薄层。例如硅胶带微酸性,有时对碱性物质如生物碱的分离不好,如不能展层或拖尾,则可在铺制薄层时,用稀碱溶液如0.1~0.5NNaOH溶液制成碱性硅胶薄层。例如猪屎豆碱在以硅胶为吸附剂时,以氯仿—丙酮—甲醇(8∶2∶1)为展开剂Rf<0.1,采用碱性硅胶薄层用上述相同展开剂,Rf值增至0.4左右。同时说明猪屎豆碱为一碱性生物碱。
④应用:薄层层析法在植物化学成分的研究中,主要应用于化学成分的预试、化学成分的鉴定及探索柱层分离的条件。用薄层层析法进行植物化学成分预试,可依据各类成分性质及熟知的条件,有针对性地进行。由于在薄层上展层后,可将一些杂质分离,选择性高,可使预试结果更为可靠。
以薄层层析法进行植物化学成分鉴定,最好要有标准样品进行共薄层层析。如用数种溶剂展层后,标准品和鉴定品的Rf值、斑点形状颜色都完全相同,则可作初步结论是同一化合物。但一般需进行化学反应或红外光谱等一种仪器分析方法加以核对。
用薄层层析法探索柱层分离条件,是实验室的常规方法。在进行柱层分离时,首先考虑选用何种吸附剂与洗脱剂。在洗脱过程中各个成分将按何种顺序被洗脱,每一洗脱液中是否为单一成分或混合体,均可由薄层的分离得到判断与检验。通过薄层的预分离,还可以了解多组分样品的组成与相对含量。如在薄层上摸索到比较满意的分离条件即可将此条件用于干柱层析。但亦可以将薄层分离条件经适当改变,转至一般柱层所采用洗脱的方式进行制备柱分离。用薄层进行某一组分的分离,其Rf值范围,一般情形下为0.85>Rf>0.05。
此外,薄层层析法亦常应用于中草药品种、药材及其制剂真伪的检查、质量控制和资源调查;对控制化学反应的进程,反应副产物的检查,中间体分析;化学药品及制剂杂质的检查;临床和生化检验以及毒物分析等,都是有效的手段。
3.聚酰胺层析(PolyamideChromatrgraphy)
聚酰胺是一类化学纤维原料,由己二酸与己二胺聚合而成的称锦纶-66,由己内酰胺聚合而成的称锦纶-6。
聚酰胺由于分子中含有多数酰胺基,在水溶液中能与酚羟基通过氢键结合而被吸附,而与不含酚羟基的化合物分离。如果化合物分子中酚羟基数目多或其活性大,则被吸附越强。从聚酰胺柱上洗脱被吸附的酚性化合物,是利用一种溶剂的分子取代酚性化合物被吸附的位置而完成的。也就是以一种新的氢键代替原有的氢键解吸附而完成的。溶剂的这种解吸附性质的强弱,一般是按下述顺序加强的。不过在使用乙醇时,其浓度亦应该逐渐加大,以利于分离。
水→乙醇→甲醇→丙酮→氯仿→稀氨水或稀NaOH水液→甲酰胺→二甲基甲酰胺→尿素水溶液
许多酚性成分包括黄酮类、羟基蒽醌等,都可应用聚酰胺柱层析得到分离。具体操作时,应将聚酰胺颗粒研磨成小于100目的细粉,并预先将聚酰胺粉混悬于水中湿浸装注。在洗脱时,溶剂性质改变不宜过快。如中药虎杖中的虎杖甙(Polydatin),就是以虎杖的醇提取物通过聚酰胺柱,先以大量水洗去不含酚羟基的成分,然后以20%乙醇洗脱虎杖甙。
4.纸层析(PaperChromatography,PC)
纸层析是20世纪40年代中期在柱层析基础上发展起来的一种微量分析方法。在大多数情况下,它是属于液-液分配层析。一般滤纸有较强的引湿性,干燥的滤纸本身就有6%~7%的水,这些水分是通过氢键与纤维素上的羟基相结合。当将它置于饱和的水汽中时,滤纸的表面吸附与毛细作用可吸收达20%~25%的水分。通常把吸附在滤纸上的水看作为一个相即固定相,而滤纸纤维则是起到一个惰性支持物的作用。层析时通常是选用一种有机溶剂,例如水饱和的正丁醇,或以水饱和的酚来展层,称为流动相。将某一个被分离物质滴加在滤纸的一端,通常距纸底端3~4cm左右划一线(称起始线),在线上作一“×”号表示点样的位置,各点之间的间距约为2cm左右,样品浓度为mg/mL,点的直径在0.2~0.3cm。
(1)滤纸的选择与处理:层析用滤纸必须是质地均匀、平整无折痕,保证溶剂展开时速度均匀,并应具一定机械强度,以免被溶剂湿润后而折倒,还应保持一定的纯度。杂质过多往往影响层析结果,如重金属的存在对氨基酸、有机酸、酚类物质的分离都是不利的。滤纸可因质地松紧厚薄的不同,而使溶剂在通过滤纸时有快速、中速、慢速之分。因此,有各种规格类型的滤纸。对滤纸的选择应结合分离对象加以考虑。对Rf值相差很小的化合物,应采用慢速滤纸;对Rf值相差较大的样品混合物,宜用快速滤纸;一般情况以选用中速滤纸为宜。至于对滤纸厚度的选用,作一般定性分析时可用薄型滤纸,若作定量或制备时则以选用厚型为宜。
滤纸中若有多量重金属离子存在时,可用0.4N盐酸水溶液将滤纸浸渍24h,用水漂洗去酸液,然后用乙醇乙醚洗涤,平整置于30℃烘箱内干燥,即可供应用。
(2)溶剂系统的选择:用于分配层析的溶剂系统,多数采用与水能部分相溶的有机溶剂,如水饱和的正丁醇或酚—水(8∶2)等。溶剂系统的选择原则是;溶剂系统的亲水性或亲脂性应该和被分离样品的亲水性或亲脂性相适应。例如对一个极性物质而言。当用水饱和的正丁醇为展开剂时,Rf值低于0.1,此时欲提高该物质的Rf值,可用增加有机相中的含水量来提高极性物质的Rf值。方法之一是在与水部分相溶的有机溶剂中,加入有机酸或有机碱,就能促使与水的混溶度增加,因而提高Rf值。如常用的正丁醇—醋酸—水(4∶1∶1)。
对某些化合物尤其是弱酸与弱碱,它们的解离度受溶剂系统pH影响较大。解离度大、极性强,Rf值就小。因此,改变溶剂系统的pH值,会显著影响Rf值。如氨基酸的纸层离,在溶剂系统中加入氨后,可使酸性氨基酸的Rf值降低,碱性氨基酸的Rf值增大。
对一些亲脂性较强的样品,在以水为固定相的纸层析中,可能随流动相到达滤纸的前沿。Rf值近于l,或者反之留在原点不动Rf值近于零,都不能达到分离要求。前者说明溶剂系统的亲脂性太强,后者的亲脂性又太弱。这就需要调节溶剂系统的组成,或改用非水而又亲水性的溶剂如甲酰胺、丙二醇等代替水作为固定相,以使分离的效果得到改善,化合物在纸上移动距离适中,Rf值在0.3~0.7范围内。加固定相的方法是将甲酰胺或丙二醇溶解在丙酮中,配成20%~30%的溶液,再将滤纸条浸入溶液中,立即取出,置两层粗滤纸间压平,以吸除滤纸条表面上多余的溶液。取出滤纸条让丙酮挥发,甲酰胺或丙二醇即均匀地留在滤纸纤维中。滴加样品后,用以甲酰胺或丙二醇饱和的亲脂性溶剂作流动相进行层析即可。纸上固定相含量的多少,可用不同浓度固定相的丙酮溶液来调节。如欲分离的样品亲脂性太强,则需应用反相层析。可用液体石蜡或凡士林的苯溶液为固定相,而用亲水性较强的溶剂(需经固定相饱和)为流动相。
(3)纸层析的应用;纸层析用作微量的分析,特别适合于亲水性较强的成分,其层析效果往往比吸附薄层层析好。但纸层析一般需要较泛的时间。例如正丁醇—醋酸—水(4∶1∶5)上层为流动相,展层25~30cm需12~15h,且纸上显色不能应用腐蚀性强的试剂,这些都不如薄层层析法优越。
5.大孔吸附树脂法(mscroporousabsorptionresin)
大孔吸附树脂法是20世纪70年代以来发展起来的有机高聚物吸附剂,具有较好的吸附性能。它的吸附作用是通过表面吸附、表面电性或形成氢键。常见的大孔吸附树脂,是一种不含交换基团的、具有大孔结构的高分子吸附剂。主要是以苯乙烯、二乙烯苯为原料,在0.5%的明胶水混悬液中,加入一定比例的致孔剂聚合而成。目前常用的为苯乙烯型和丙烯腈型。它的理化性质稳定,不溶于酸、碱及有机溶剂;对有机物的选择性较好,不受无机盐类及强离子低分子化合物存在的影响。
大孔吸附树脂较之凝胶树脂及天然吸附剂有吸附容量大、选择性好、易于解吸附、机械强度高、再生处理简便、吸附速度快等优点,特别适合于从水溶液中分离低极性或非极性化合物。近年来在抗菌素、生化药物的提取分离中受到普遍重视。
其主要用途是用于分离、脱盐、浓缩及去除有机杂质。
(1)脱盐:采用低极性大孔树脂,可同时去除阳离子、阴离子,并且不改变溶液的pH,较离子交换树脂脱盐有明显优点。例如将碱性水溶液的氨基糖甙,通过大孔吸附树脂,氨基糖就能形成集中的吸附带,而盐溶液则快速通过树脂柱,去盐后可用10%~20%含水醇或丙酮洗脱吸附物。
(2)分离:组分间极性差别越大,分离效果越好。混合组分在大孔树脂吸附后,一般可依次用水、含水醇、酮,10%~20%v/v洗脱,最后可用浓醇或酮洗脱。
目前更有应用大孔树脂直接从微生物的发酵液进行吸附提取抗菌素。直接从水溶液中吸附提取分离低极性有效成分,能减少有机溶剂的用量并简化工艺,是值得重视的。
(四)根据有机化合物相对分子质量差别进行分离
常用的有透析法、凝胶过滤法、超滤法等。前两者是利用半透膜的膜孔或凝胶的三维网状结构的分子筛过滤作用;超滤法则是利用因分子大小不同引起的扩散速度的差别。以上这些方法主要用于水溶性大分子化合物,如蛋白质、核酸、多糖类的脱盐精制及分离工作,对分离小分子化合物来说不太适用。而凝胶过滤法也适用于分离相对分子质量1000以下的化合物。
1.透析法
透析法是利用小分子物质在溶液中可通过半透膜,而大分子物质不能通过的性质以达到分离的目的,如图2-4所示。例如分离纯化皂甙、蛋白质、多肽、多糖等大分子成分时,可用透析法除去小分子杂质如无机盐、单糖、双糖等。透析法是否成功与透析膜的规格关系极大。透析膜的膜孔有大有小,要根据欲分离成分的具体情况而选择。透析膜有动物性膜、火棉胶膜、羊皮纸膜(硫酸纸膜)、玻璃纸膜、蛋白胶(明胶)膜等。通常可用市售的玻璃纸或动物性膜扎成袋状,小心加入欲透析的样品溶液,放入清水缸中,经常交换缸内的水,使透析速度加快。透析是否完全,可取透析膜内的溶液进行分析即知。

图2-4 透析法示意图
透析法分离的速度较慢,为了加速透析速度,可用电透析法,即在纯溶剂中,傍近半透膜放置电极,如图2-5所示,加上电压,即可使带电荷的离子的透析速度增加10倍以上。
2.凝胶过滤法(gelfiltration)
(1)基本原理:凝胶过滤法(gelfiltration)也叫凝胶渗透层析(gelpermeationchromtograghy)或分子筛过滤(molecularsievefiltration),系利用分子筛分离物质的一种方法。其中所用载体,如葡聚糖凝胶,是不溶于水,但可在水中膨胀的球形颗粒,具有三维空间的网状结构。葡聚糖凝胶在吸水后形成凝胶粒子,在其交链键的骨架中有许多一定大小的网眼。网眼大,大分子物质能进入网眼内;网眼小,只有小分子物质才能进入网眼。而超过一定限度的大分子物质,就被排阻在凝胶粒子的外部,不能进入网眼。这就使得能进入凝胶内部与不能进入凝胶内部的分子,如同按照分子大小过筛一样,所以称为分子筛。操作时首先将凝胶在适宜的溶剂中浸泡,使其充分膨胀,然后装入层析柱中。加入样品后,再以同一溶剂洗脱,则样品中大分子化合物不能进入凝胶颗粒内部,只在凝胶颗粒间移动,因此阻力小,行动快,走在前面。而小分子化合物能自由扩散进入到凝胶内部,因此通过层析柱时受到阻力大,行动慢,走在后面。如此经过—段时间的洗脱,混合物中各个组分就会按照分子的大小而获得分离。
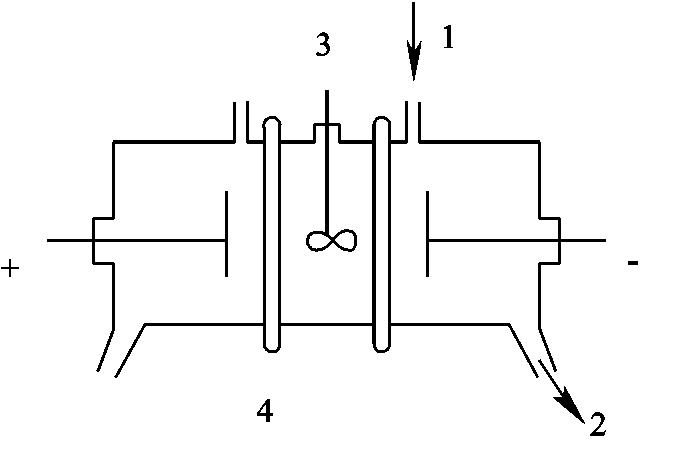
图2-5 电透析示意图
1.纯溶剂进口;2.出口;3.搅拌器;4.半透膜
(2)凝胶的类型:常用的凝胶有葡聚糖凝胶(SephadexG)及羟丙基葡聚糖凝胶(SephadexLH-20)。
葡聚糖凝胶:葡聚糖凝胶也称交链葡聚糖凝胶,是由葡聚糖(右旋糖苷)和甘油基通过醚桥(—O—CH2—CHOH—CH2—O—)相交链而成的多孔性网状结构。商品凝胶是干燥的颗粒状物质,在使用前必需使其充分溶胀。由于葡聚糖分子内含有大量羟基而具有极性,在水中即膨胀为凝胶粒子。它不溶于水及盐溶液,在碱性或弱酸性溶液中稳定(在强酸中通高温可使糖甙键水解)。葡聚糖凝胶“网眼”的大小,可在制备时加以控制,添加不同比例的交链剂,可获得交链度不同的凝胶。交链度越大,网状结构越紧密,孔隙越小,吸水时膨胀也越少。反之,交链度越小,网状结构越疏松,孔隙越大,吸水时膨胀亦越大。
根据被分离物质的分子量大小可选用不同型号的凝胶。交链度大、孔隙小,可用于小分子量物质的分离。交链度小、孔隙大,则用于大分子量物质的分离。商品上凝胶的型号一般是按交链度大小来分类,并以吸水量或膨胀量即每克干凝胶所吸收的水分重量来表示。如G-25的吸水量为2.5mL/g。
羟丙基葡聚糖凝胶:它是在SephadexG-25分子中引入羟丙基以代替分子中羟基的氢,成醚键的结合状态:R—OH→R—O—CH2CH2CH2OH(即为葡聚糖凝胶LH-20),而具有一定程度的亲脂性,在许多有机溶剂中也能膨胀。
SephadexLH-20除具有分子筛特性,可按分子大小分离物质外,在由极性与非极性溶剂组成的混合溶剂中常常起到反相分配层析的效果,适用于不同类型有机物的分离,在植物化学成分的分离纯化方面得到了越来越广泛的应用。
使用过的SephadexLH-20可以反复再生使用,而且柱子的洗脱过程往往就是柱子的再生过程。短期不用时可以水洗→含水醇洗(醇的浓度逐步递增)→醇洗,最后泡在醇中贮于磨口瓶中备用。如长期不用,可在以上处理基础上,减压抽干,再用少量乙醚洗净抽干,室温充分挥散至无醚味后,60~80℃干燥后保存。
(五)根据有机化合物离解度不同进行分离
有些天然有机化合物分子中含有酸性、碱性及两性基团,在水中多呈解离状态,据此可用离子交换法或电泳技术进行分离。
1.基本原理
离子交换法是以离子交换树脂作为固定相,用水或与水混合的溶剂作为流动相。当流动相流过交换柱时,在流动相中存在的离子性物质与树脂进行离子交换反应而被吸附,代替了因吸附剂表面活性所产生的吸附作用,中性分子及具有与离子交换树脂交换基团相反电荷的离子将不被吸附从柱子流出,而具有相同电荷的离子则与树脂上的交换基团进行离子交换并被吸附到柱上,采用适当溶剂进洗脱,不同极性的物质按极性大小的顺序被从柱上洗脱下来,即可达到物质的分离。
2.离子交换树脂的结构及性质
离子交换树脂分为两大类,即阳离子交换树脂和阴离子交换树脂。阳离子交换树脂分子中含有活泼的酸性基团,能交换阳离子;阴离子交换树脂中含有活泼的碱性基团,能交换阴离子。按照活性基团的酸、碱性强弱,阳离子交换树脂分为强酸型(如-SO3-H+)、弱酸型(如-NH4+、-COO-H+);阴离子交换树脂有强碱型[如-N+(CH3)3Cl-]、弱碱型[如含RCH2N(CH3)2]和中等碱型。
离子交换树脂是一种高分子化合物,外观均为球形颗粒,不溶于水,但可在水中溶胀。它由树脂核和离子交换基团两个部分组成。离子交换树脂的树脂核,是由苯乙烯通过二乙烯基苯交链聚合而成。二乙烯基苯在离子交换树脂中所占的重量百分比称为“交链度”。如国产树脂732(强酸1×7),其中l×7即表示交链度是7%。
交链度可反映柯帖的网眼大小。交链度越大,树脂内的孔洞就越小,大分子物质就不易进入树脂颗粒之内。例如分离氨基酸或小分子肽(二肽或三肽),则以8%交链度的树脂为宜。而对分子量较大的肽,则可选用4%~2%交链度较小的树脂为适宜。一般只要不影响分离的完成,以采用交链度较高的树脂为适宜。因为交链度高,网眼小,组成紧密,性质较稳定,不易破坏,寿命长。但由于网眼上分子小的离子可进去,分子大的离子进不去,也就是交换不上,表现为交换容量小,而选择性强。
3.离子交换树脂的再生
离子交换树指使用一段时间后,就会失去交换能力,这时,就需要进行“再生”处理。“再生”处理就是用强的无机酸或碱溶液浸泡已失去交换能力的交换树脂,使其发生离子交换反应的逆过程,即用H+或OH-再将树脂上的阳离子或阴离子交换出来。通常用盐酸或硫酸溶液“再生”处理阴离子交换树脂,用氢氧化钠溶液“再生”处理阳离子交换树脂,用氢氧化钠溶液“再生”处理阴离子交换树脂。经过“再生”处理的离子交换树脂洗净后可继续使用。
4.离子交换树脂法应用
(1)用于不同电荷离子的分离。可对植物水提取物中的酸性、碱性及两性化合物进行有效的分离。
(2)用于相同电荷离子的分离。基于被分离物质的碱性强弱不同进行分离。但对于电荷相同、解离度近似的混合物来说,一级的离子交换方法难以达到良好的分离效果,而须用离子交换层析法。其原理与离子交换树脂法相同,关键在于选好固定相(树脂)及流动相(缓冲液)。所用树脂须根据待分离物质的稳定性、解离基的类型及强度(pKa),进行选择,并须进行干燥、粉碎、浮选其中200~400目左右的微粒供用。而流动除了用磷酸盐缓冲液外,还采用有机酸(甲酸、乙酸)、碱(如吡啶、2-甲基吡啶、3-甲基吡啶、N-乙基吗啉)做成的缓冲液,以便在减压浓缩或冷冻干燥时除去。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。














