一、地中海贫血
人类血红蛋白各种类型在个体发育的不同阶段先后出现,并且相互交替:在胚胎发育早期,合成胚胎型血红蛋白(HbGower1、HbGower2和Hb Portland);在胎儿期,主要合成胎儿型血红蛋白HbF;成人期则是成人型血红蛋白HbA和HbA2(表15-2),这是由于编码这些珠蛋白的基因随着个体发育的进程有规律地依次开启和关闭。在另一方面,合成珠蛋白的特异性组织器官也依个体发育的不同阶段而不同,分别为卵黄囊、胎肝和骨髓。血红蛋白合成在个体发育中所出现的变化,反映了珠蛋白基因表达的时空变化既精确又协调。
表15-2 人体发育各阶段血红蛋白的组成

珠蛋白基因结构和表达异常导致各种珠蛋白链合成变化是引起地中海贫血的分子基础。
(一)珠蛋白生成障碍性贫血(地中海贫血、thalassemia,简称地贫)的类型
α珠蛋白链合成减缺的地贫称为α-珠蛋白生成障碍性贫血(α地贫);β链合成减缺的地贫称β地中海贫血(β地贫);γ链合成减缺的地贫称为γ地中海贫血(γ地贫);δ和β链合成减缺的地贫称为δβ地中海贫血(δβ地贫),以此类推。
按照珠蛋白链合成速率降低的程度,地中海贫血又可以区分为不同的类型。例如在α地贫中,如果同1条16号染色体上的2个α珠蛋白基因均不能表达使α链的合成完全缺乏,称为α0地中海贫血(过去称为α地贫1);如果只有1个α珠蛋白基因表达使α链部分合成,称为α+地中海贫血(过去称为α地贫2)。由这2种地贫基因可以组合成各种不同的综合征:α0地贫基因纯合子(α0地贫/α0地贫)完全不能合成α链,而合成Hb Bart’s(γ4),导致死胎、死产或新生儿死亡,称为Hb Barts胎儿水肿综合征(Hb Bart’s hydrops fetalis);α0地贫和α+地贫基因双重杂合子(α0地贫/α+地贫)只有少量α链合成,多余的β链聚合成HbH(β4),导致一种溶血性贫血病,称为HbH病(HbH disease)。同样,完全不能合成β的链的称为β0地中海贫血(β0地贫),能部分合成β链的称为β+地中海贫血(β+地贫)。β0地贫基因纯合子(β0地贫/β0地贫)以及β0地中海贫血和β+地中海贫血基因的双重杂合子(β0地贫/β+地贫)都表现严重的溶血性贫血症状。对地中海贫血的分子生物学研究表明,患者珠蛋白链合成的缺乏是由于相应的珠蛋白基因缺失或者发生点突变所致。
(二)珠蛋白基因突变类型
1.单个碱基替代 是最常见的突变类型,见于绝大多数β地中海贫血。
2.移码变异 是由于珠蛋白基因中发生1、2个碱基丢失或嵌入,致碱基排列依次位移,产生移码突变,严重改变珠蛋白肽链的结构或合成速率。
3.密码子的缺失和嵌入 在细胞减数分裂时,同源染色体发生错配或不等交换,生成缺失或嵌入密码子,形成异常珠蛋白基因或融合基因并表达异常珠蛋白链。某些珠蛋白链由2种不同的肽链衔接而成。例如Hb Lepore由δ和β链连接而成,其N端像δ链,C端像β链,称δβ链。与此相反,反-Lepore,其N端像β链,C端像δ链,称为βδ链。这是由于染色体的错误联合和不等交换,形成了融合基因的δβ和βδ,合成了融合链的血红蛋白。β和δ基因的融合意味着β基因域的缺失,合成β链减少,表现为β地中海贫血的临床症状。
4.无义突变 珠蛋白基因中正常密码子突变为终止密码子,蛋白链合成便提前终止。
5.终止密码突变 珠蛋白基因的终止密码子(UAA、UAG或UGA)发生突变,珠蛋白链的合成不在正常位置上终止,继续合成至新的终止密码子,生成延长的异常珠蛋白链。
6.基因缺失 基因的部分顺序或整个基因缺失,如α-珠蛋白基因缺失导致不同类型的α-地中贫血。
(三)地中海贫血的基因诊断
1.α地中海贫血(α地贫) α珠蛋白基因缺失是引起α地贫的分子基础。人类16号染色体短臂中2个α珠蛋白基因(α2和α1基因)、胚胎期功能基因ξ2和3个非功能基因ψζ、ψα2和ψα1以及尚未知功能的θ基因成簇排列。α珠蛋白基因之间存在着高度同源性,在减数分裂时同源染色体之间可产生错位配对,引发不等交换,导致α珠蛋白基因簇不同程度的缺失和α珠蛋白基因数目的增多(图15-3)。缺失型α地贫所缺失的基因(DNA)长短和部位都不相同,以致缺失型α地贫有20多种。

图15-3 α珠蛋白基因不同程度的缺失和增多
(1)α珠蛋白基因缺失的长短和范围中国人中α珠蛋白基因缺失的类型主要有3种:①东南亚缺失型:α2和α1珠蛋白基因都缺失,完全不能表达α链的合成,故相当于α0地贫。②右侧缺失型:缺失α2珠蛋白基因的3′端和α1珠蛋白基因的5′端,形成由α1基因的3′端和α2基因的5′端构成的融合基因,缺失片段的大小约为3.7kb。基因型为α-3.7/。右侧缺失型α地贫中,由于同一条16号染色体上仍保留了由α2珠蛋白基因的5′端(包括启动区)和α1珠蛋白基因的3′端构成的一个完整的α珠蛋白基因,故相当于α+地贫。③左侧缺失型:整个α2珠蛋白基因缺失,但α1珠蛋白基因保持完整,缺失片段的长度为4.2kb,基因型为α-4.2/。此型也相当于α+地贫。但是由于α2珠蛋白基因的表达水平占整个α珠蛋白基因表达量的70%左右,因此,理论上左侧缺失型α地贫要比右侧缺失型α地贫严重。
部分α地贫是由α珠蛋白基因的点突变所致。我国发现的α地贫点突变只有2种:一种是Hb constant spring(HbCS),α2珠蛋白基因的第142位终止密码子TAA突变成编码谷氨酰胺的CAA,肽链处延合成到173位的第2个终止密码子结束;另一种是Hb广西(Hb Quong Sze),α2珠蛋白基因第125位密码子突变使原来编码亮氨酸变为编码脯氨酸所致。由于引起HbCS和Hb广西点突变均发生在表达占优势的α2珠蛋白基因,因此引起的α地贫的症状较重。
(2)常用的α地贫的基因诊断技术
1)DNA点杂交:把患者DNA直接点加在硝酸纤维薄膜上,与放射性核素标记的α珠蛋白基因探针作杂交。根据杂交斑点的放射强度,即能鉴定出α珠蛋白基因是否缺失以及缺失的数目。也可用PCR扩增DNA,用点杂交进行分析。
2)RFLP分析:是基因诊断α地贫的基本方法,常用的限制性内切酶为Bam HⅠ和BglⅡ以及Eco RI(表15-3)。
表15-3 RFLP分析诊断α珠蛋白基因异常

注:*表中所列数字为DNA序列长度,单位为kb。
3)PCR分析:α珠蛋白基因簇内的DNA序列存在着很高的同源性,尤其是α2和α1珠蛋白基因的序列几乎完全同源,PCR不宜应用于α地贫的基因诊断。
2.β地中海贫血(β地贫) β地贫绝大多数是由于β珠蛋白基因不同类型的点突变,包括单个碱基的取代,个别碱基的插入或缺失导致转录异常,mRNA前体剪接加工错误,翻译无效,或合成不稳定的珠蛋白链,使α、β珠蛋白链不平衡或阻碍α2、β2四聚体形成。全世界已发现200余种β地贫,中国内地有21种(表15-4)。
表15-4 中国人β地贫突变基因类型

续表

β地贫基因的类型以及分布频率具有明显的种族特征和地域差异。β珠蛋白基因第41-42密码子的移码突变CD41-42(-TCTT),第二内含子654C→T,第17密码子无义突变CD17A→T,启动子区TATA盒中-28A→G,第71-72密码子的移码突变CD71-72(+A),以及HbE等6种β地贫基因占中国人所有β地贫基因的90%以上。不同β地贫基因在不同地区分布频率不同。华南:最常见的是CD41-42(-4bp),占47.1%,IVS-2nt654C→T占23.6%。西南:CD17A→T占33.3%,IVS-2NT654C→T占20.6%。华东:CD41-42(-4bp)占33.8%,CD71-72(+A)占24.6%。台湾:IVS-2nt654C→T占38.7%,CD41-42(-4bp)占24.6%。不同民族间也有差异。壮族人与汉族人所具有的β地贫基因谱相似。海南黎族人β地贫基因几乎完全为CD41-42(-TCTT),高达94.7%。云南西南部德宏地区的阿昌族,人口总数不足3万,HbE的基因频率高达41.2%。新疆维吾尔族人群中发现了CD8(-AA)和CD8-9(+G)等中亚、南亚地区常见的β地贫突变类型,前者的基因频率达16.6%。
β地贫患者的β珠蛋白基因并不缺失,而是基因点突变、碱基插入或缺失,这些突变往往不涉及基因的限制性内切酶的识别位点,因而不采用限制酶的酶谱分析或PCR检测基因的缺失,而是应用RFLP连锁分析间接检测β地贫基因,或者应用寡核苷酸探针直接检测和鉴定β地贫基因。
(1)RFLP连锁分析 对于一些突变型未知的β地贫患者和他们的家庭成员的β基因组作PCR扩增再行RFLP连锁分析,是对风险胎儿进行产前诊断的有效手段。作者实验室应用7种探针对中国人β珠蛋白基因簇中的13个RFLP位点进行了分析,获得中国人RFLP的资料(表15-5)。分析结果表明,中国人β珠蛋白基因簇中存在着广泛的RFLP多态性,与其他国家民族的β珠蛋白基因簇有一定的差异。
应用RFLP连锁分析对β地贫风险胎儿进行产前诊断时,可有完全诊断、50%诊断或完全不能诊断,这取决于家庭成员中是否有杂合性,对杂合频率较高的RFLP位点作分析,可提高产前诊断率。
PCR与RFLP连锁分析组合,不需Southern印迹杂交、不需非放射性核素,适用于高危胎儿的产前诊断。例如,从表15-6获知,在β珠蛋白基因5′处有限制性内切酶Hgi AI的RFLP位点,频率近于0.5,可作遗传标记。通过PCR扩增含Hgi AI酶切位点的110bp片段,用Hgi AI消化,具有RFLP多态位点的被切割成65+45bp两种片段,经凝胶电泳分析,可观察到这些酶介片段,然后在家庭中进行RFLP连锁分析即可对胎儿进行产前诊断。例如,父亲和母亲均具有110/65+45bp的片段,患儿为110bp的片段,表明110bp与β地贫基因连锁,如果胎儿为65+45bp片段而没有110bp片段,则可产前诊断胎儿正常。如只有110bp而没有65+45bp,胎儿应为β地贫患者,如同时出现110bp/65+45bp,胎儿为杂合子。
表15-5 β珠蛋白基因簇的RFLP资料及不同民族之间的比较
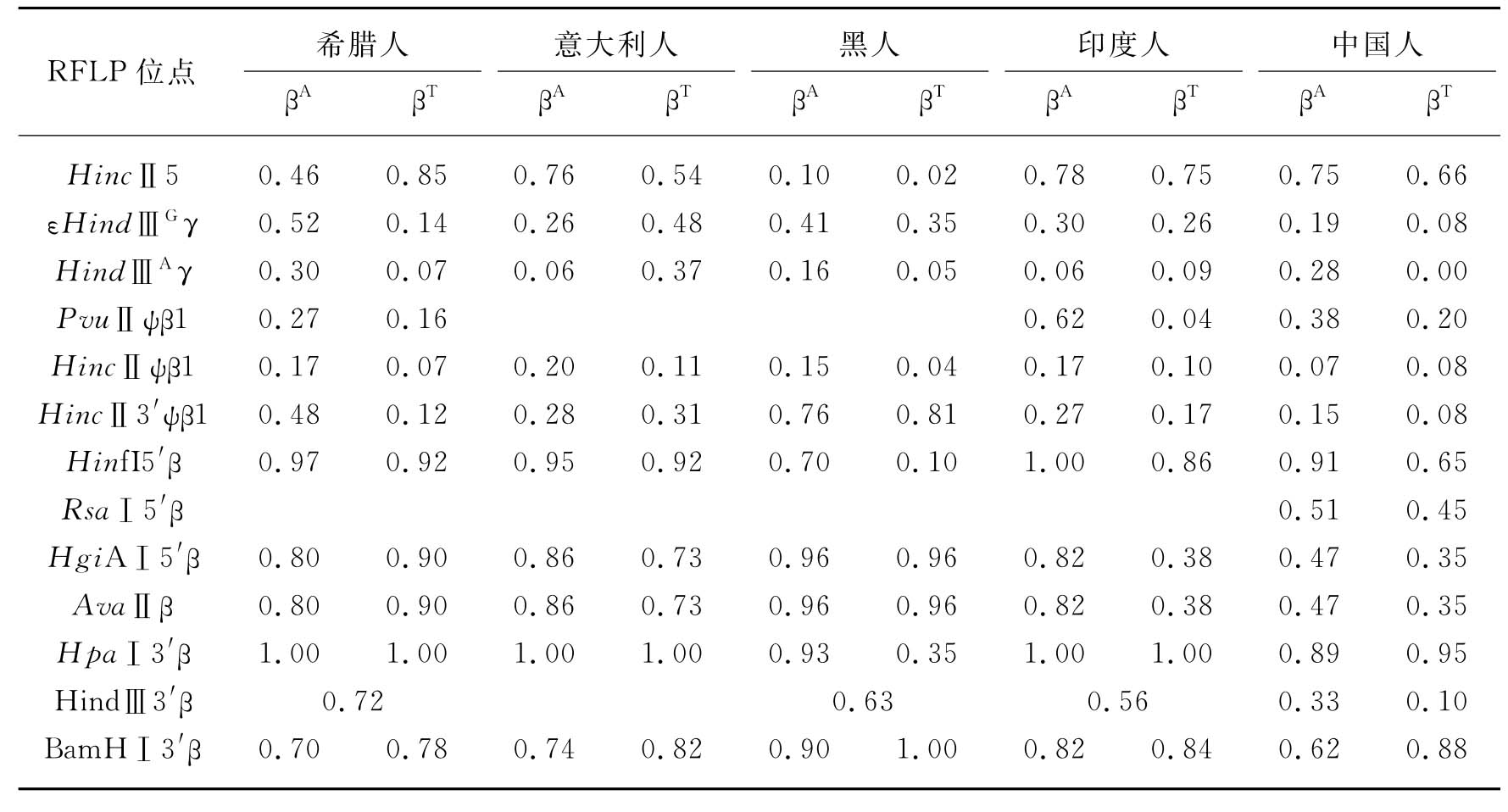
表15-6 10组检测β地贫突变的ASO探针

注:①M:突变探针序列;②N:相应的正常探针序列。
(2)PCR/ASO探针分析 各民族或群体具有独特的β地贫基因型,因此,合成本民族特异的突变及其相应的正常的等位基因寡核苷酸(allele-specific oligonucleotide,ASO)探针,长度为19个碱基,用γ-32P ATP作末端标记,与PCR扩增的β珠蛋白基因片段进行杂交,放射自显影后,诊断受检者是否为突变的纯合子或杂合子或者完全正常(图15-4)。合成10组ASO探针,分别特异于TATA盒-29A→G,TATA盒-28A→G,CD14-15(+G),CD17A→T,IVS-Int 1G→T,IVS-Int5G→C,CD41-42(-4bp),CD43G→T,CD71-72(+A)和IVS-2-654C→T等10种中国人β地贫基因(表15-6)。用于扩增β珠蛋白基因的两对引物序列为:5′-GTACGGCTGTCATCACT-TAGACCTCA-3′,5′-TGCA GCTTGTCACAGTG-CAGCTCACT-3′和5′-GTGTACACATATTGAC-CAAA-3′,5′-AGCACACAGACCAGCACGTT-3′,它们分别扩增601bp和422bp的珠蛋白基因片段。前者包含除IVS-2nt.654以外的9种β地贫突变位点,后者仅包含IVS-2nt.654突变位点。

图15-4 PCR/ASO探针法检测IVS-2-654C→T突变
N:正常探针,M:IVS-2-654C→T突变探针。N和M两张膜同一位置的斑点表示同一样品分别用N和M探针杂交的结果。若N阳性而M阴性,表示该样品无这种突变;若N和M均阳性,表示该样品为这种突变的杂合子;如N阴性而M阳性,表示样品为这种突变的纯合子。
PCR/ASO探针分析一般能满足β地贫基因诊断和产前诊断,但ASO探针杂交分析只能针对一种突变,完成一次基因诊断需要多次重复的ASO探针杂交。反向点杂交(reverse dot blot,RDB)技术是把一组特异于β地贫基因的ASO探针固定在一张膜上,用此膜与扩增的β珠蛋白基因片段进行杂交,一次杂交就可同时检测一组β地贫的突变。其技术关键是调整各探针长度和选择正负链,使其Tm值尽量接近,使杂交和洗膜条件一致。
(3)多重等位基因特异性PCR(multiplex allelic specific PCR,MAS PCR)分析 对中国人中发病率最高的5种β地贫突变类型:-28A→G,CD41-42(-4bp),CD17A→T,CD71-72(+A)和IVS-2-654C→A,设计和合成五组扩增引物。通过适当的组合和调整组成一个多重等位基因特异性PCR(MASPCR)体系,仅用一次PCR就可检测这5种不同的β地贫突变基因。其技术特点是在每一个PCR体系中,包括特异于-28A→G、CD17A→T、CD41-42(-4bp)、CD71-72(+A)及IVS-2-654C→T这5种β地贫突变位点的等位基因特异引物,并把突变基因与正常等位基因所不同的那一个或几个碱基设计在这些引物的3′端(表15-7,图15-5),根据C/N和C/M反应体系是否产生相应的特异长度扩增带,可以直接判断样品中是否有该种突变,是杂合子还是纯合子(图15-6)。工作量和试剂用量大大减少,同时共用引物一经PCR扩增1434bp恒定扩增带作为内对照,该条带的有无可作为MASPCR成功与否的标志,排除假阴性结果。MASPCR技术值得向临床推广应用。
表15-7 应用于检测β地贫基因的MASPCR寡核苷酸引物

注:①N:正常序列引物,3′端碱基对应于正常DNA序列;②M:突变序列引物,3′端碱基对应于突变DNA序列;③C1,C2:共同引物序列,分别与N或M配合使用。
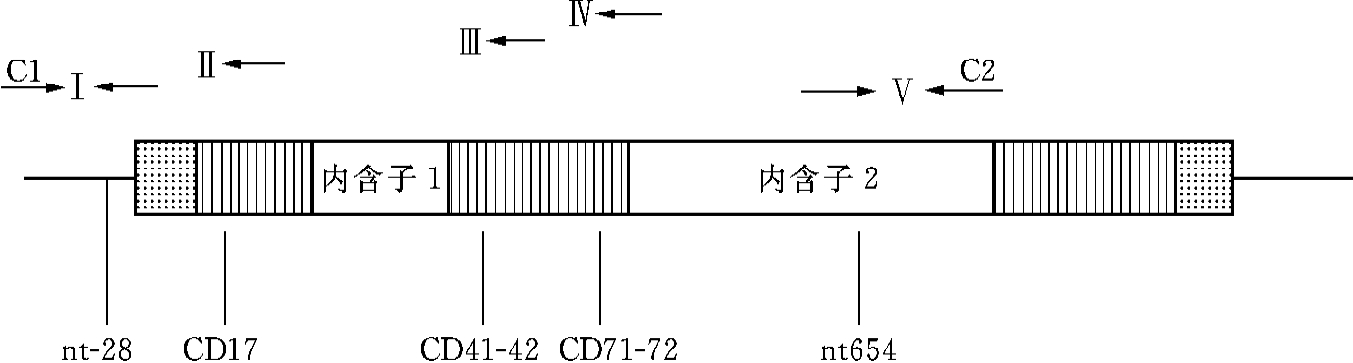
图15-5 应用MASPCR基因诊断β地中海贫血的示意图
Ⅰ:特异于-28A→G突变类型的寡核苷酸引物及其扩增区域;Ⅱ:特异于CD17A→T突变类型的寡核苷酸引物及其扩增区域;Ⅲ:特异于CD41-42(-4bp)突变类型的寡核苷酸引物及其扩增区域;Ⅳ:特异于CD71-72(+A)突变类型的寡核苷酸引物及其扩增区域;Ⅴ:特异于IVS-2-654C→T突变类型的寡核苷酸引物及其扩增区域
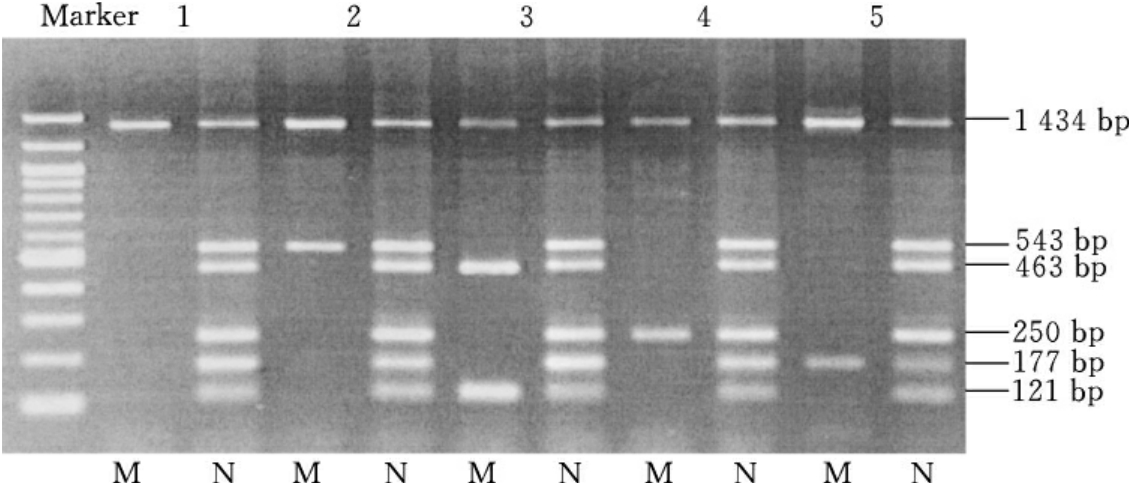
图15-6 MASPCR基因诊断β地中海贫血的凝胶电泳分析
Marker:123bp DNA分子质量标记;M:5对C/M引物的MASPCR;N:5对C/N引物的MASPCR。1:正常人;2:CD71-72(+A)杂合子;3:CD41-42(-4bp)/IVS-2-654C→T双重杂合子;4:CD17A→T杂合子;5:IVS-2-654C→T杂合子
(4)未知突变类型β地贫的基因诊断 对于未知突变类型β地贫,除可采用RFLP连锁分析进行间接基因诊断外,主要依赖于PCR结合变性或温度梯度凝胶电泳(DGGE或TGGE)和单链多态构象多态性(SSCP),将未知突变锚定在一定的DNA片段内,然后进行DNA序列测定。β地贫表型的突变位点可能位于β珠蛋白基因远端的调控序列,或者根本不与β珠蛋白基因连锁,甚至不在第11号染色体上,基因诊断时十分困难。
(5)地贫的RNA诊断 在α地中海贫血个体中,α珠蛋白mRNA的含量随α珠蛋白基因的缺失而减少;在β地中海贫血患者中,正常的β珠蛋白mRNA显著减少(β+)或缺失(β0)。通过分析有核红细胞α和β珠蛋白mRNA,可以有把握地对α或β地中海贫血进行诊断和鉴别诊断。以RT-PCR技术定量测定受检对象对周血有核红细胞中各种珠蛋白mRNA含量,可对各型地贫进行基因诊断(表15-8)。
表15-8 地贫患者珠蛋白mRNA测定(x-±s)

3.中间型β地中海贫血 临床表现较轻的β地贫类型,约占β地贫病例总数的10%。中间型β地贫的发生不仅涉及β珠蛋白基因,还涉及整个β珠蛋白基因簇或α珠蛋白基因簇,甚至与非珠蛋白基因的变异有关。
中间型β地贫的分子基础主要有:
(1)β地贫基因杂合子复合α珠蛋白基因的增多 这类患者有一个β地贫基因,5个甚至6个α珠蛋白基因,产生α链与非α链之间的不平衡,表现为中间型β地贫。α珠蛋白基因数目增多的单体型可分成左侧不等交换型增多(αααanti4.2)和右侧不等交换型增多(αααanti3.7)。
(2)β地贫基因纯合子或双重杂合子复合α珠蛋白基因减少 作者实验室的一组14例中间型β地贫患者中,有3例属于β地贫基因双重杂合子复合α珠蛋白基因数目的减少。在α珠蛋白基因和β珠蛋白基因异常的高发地区,同一患者可能同时存在2种不同珠蛋白基因簇异常。
(3)典型β地贫基因与静止型β地贫基因双重组合 静止型β地贫基因(silentβ-thalas-semia allele)是指β珠蛋白基因的突变存在于单纯的杂合子状态,完全无临床症状,血液学检查也正常,只有通过非常灵敏的珠蛋白mRNA分析才能发现其β珠蛋白mRNA的表达有轻微的异常。这些突变与典型的β地贫基因组合在一起形成复合杂合子,则β珠蛋白基因的表达受到明显的影响,出现中间型β地贫临床症状。常见的两种静止型β地贫基因是β珠蛋白基因5′端上游CACCC盒nt.-101C→T和5′端远端nt.-530区域基序(motif)(AT)xTy重排。nt.-101C→T突变随着从胎儿到成人的不同发育时期对β珠蛋白基因表达的影响程度也逐渐由强转弱,-530某种重排变异与某些特定的β-珠蛋白基因突变共同出现而形成双重杂合子,对β珠蛋白基因的表达发生明显影响,导致β地中海贫血。β珠蛋白基因上游-610~-490区域是反式作用因子BP1的结合部位。BP1是一种阻遏核蛋白,可抑制β珠蛋白基因转录,导致β地中海贫血。
(4)β地贫基因纯合子或双重杂合子复合γ珠蛋白基因的突变 γ珠蛋白基因是胎儿时期表达的主要非α珠蛋白基因,出生后表达水平极低,但在少数情况下,由于Gγ或Aγ珠蛋白基因启动子区域突变,使γ链在成人时期仍持续表达。基因突变与β地贫基因纯合子或双重杂合子复合存在,γ链的合成增加可代偿β链合成的不足,改善了与非α链的不平衡,使原来重型β地贫的表型转变为中间型β地贫的表型。中国人中,Gγ-158C→T和Aγ-196C→T是两种较常见的引起成人期γ链持续表达的突变类型。
(5)LCR区的片段缺失β -珠蛋白基因簇调控制区(locus control region,LCR)大片段的DNA序列的缺失亦导致β-地中海贫血。某些中间型β地贫,β珠蛋白基因(包括LCR和3′端非翻译区)的序列分析只发现一个β地贫基因,而α和γ珠蛋白基因均无异常。可能是珠蛋白mRNA加工或翻译调控的失调影响了珠蛋白基因的表达。
中间型β地贫的分子基础较为复杂,进行基因诊断时必须从多方面考虑,除了对β地贫突变类型作鉴定外,还需要对β珠蛋白基因簇中其他相关基因以及α珠蛋白基因进行分析,才有可能对中间型β地贫作出较完整的基因诊断。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。















