类质同象概念
矿物晶体结构中,某种质点(原子、离子或离子团、分子)的位置被性质相似的质点所替换,这些替换只仅仅引起晶体晶格常数、物理性质、化学性质发生有规律的变化,而晶体的晶格类型(包括键性和结构类型)不发生质变的现象被称为类质同象。
类质同象现象在矿物晶体中十分发育,在自然界比较常见。例如橄榄石晶体就是由Fe2+与Mg2+形成的一个类质同象系列,在晶体中,Fe2+与Mg2+之间可以任意发生相互替换,可形成各种Fe、Mg含量不同的类质同象混合物,如形成镁橄榄石Mg2[SiO4]-镁铁橄榄石(Mg,Fe)2[SiO4]-铁镁橄榄石(Fe,Mg)2[SiO4]-铁橄榄石Fe2[SiO4]系列。
在这个系列中,矿物的晶体结构类型相同,只是从左向右晶格常数、矿物的密度有规律地逐渐增大,矿物的颜色逐渐变深,透明度逐渐降低。
(二)类质同象类型
按不同划分依据,可将类质同象划分出不同种类:
1.以发生类质同象替换的组分在晶格中的替换程度可分为
(1)完全类质同象或连续类质同象。晶格中发生替换的组分可以以任意比例取代,而晶格类型不改变的替换,如前述的橄榄石晶格中发生的Mg2+与Fe2+之间替换则无比例限制,可以形成一个完整的镁-铁橄榄石系列。
(2)不完全类质同象或有限类质同象。晶格中发生替换的组分不可以连续进行,而是被限制在一定的范围内,即超越这个限制范围,晶格类型则会发生改变,形成另一种新类型。如在矿物闪锌矿晶格中,Fe2+替换Zn2+的范围被限制在小于26%以内,超越26%则替换不可能发生或会产生新晶格类型。
2.依晶格中相互替换的离子电价是否相等可分为
(1)等价类质同象替换。晶格中凡发生替换的离子电价相等者。如上述橄榄石晶格中的Mg2+替换Fe2+或Mg2+被Fe2+替换均为等价类质同象替换。
(2)不等价类质同象替换。晶格中凡发生替换的离子电价不相等者。但在替换时,为了保持晶格中电荷总的平衡,相互替换的离子的总电荷必须相等。而要实现总电荷的平衡必须采用如下方式替换:
①两对异价离子同时替换。如在长石中,Ca2+→Na+的同时发生Al3+→Si4+。即以Ca2++Al3+→Na++Si4+成对替换的方式进行,以保持总电荷平衡。
②电价高的离子与数量多的低价离子相互替换。这种替换发生的前提是晶格中存在有容纳多个低价离子的空隙,且结构比较松散的条件下才能发生。如云母晶格中3Mg2+←2Al3+;而绿柱石晶格中的Li++Ca2+→Al3+。
③较高电价的阳离子替换较低电价的阳离子时,多余的正电荷为高电价的阴离子替换较低电价的阴离子后形成多余的负电荷所平衡。如磷灰石晶格中,Ce3+←Ca2+的同时,发生O2-←F-的替换,即形成Ce3++O2-←Ca2++F-的成对替换。
④当相互替换的离子数目不相等时,为了保证晶格类型不改变,晶体结构会进行局部调整,如果替换后增加了离子数目,晶格中会出现多余的离子占位。如上述的绿柱石晶格中的Li++Ca2+→Al3+的替换。相反如替换后离子数目减少,则晶格中会出现缺位,则被称为缺席构造,如磁黄铁矿(Fe1-xS)晶格中的2Fe3+→3Fe2+出现缺位。
(三)类质同象发生的条件
在矿物晶格中,元素间发生类质同象替换是一种十分常见的现象,但原子、离子或离子团之间发生替换不是任何情况下都可以进行,它的发生是有一定条件的,它发生的条件如下:
1.内部条件
内部条件,又称为类质同象产生的内因条件。这些条件主要指原子或离子本身的性质,包括有:
(1)原子与离子半径。发生类质同象替换的原子或离子的半径应当接近。一般在电价和离子类型相同的情况下,离子在晶格中相互替换的能力是随着半径差别的增大而降低,若以r1、r2分别代表不同离子的半径,则有:
①当(r1-r2)/r2<10%~15%时,常形成完全类质同象替换。
②当(r1-r2)/r2在10%~25%时,高温下形成完全类质同象替换;低温下形成有限类质同象替换。
③当(r1-r2)/r2在>25%~40%时,高温下形成不完全类质同象替换;低温下不发生类质同象替换。
(2)离子的电价。在类质同象替换中,必须遵守电价平衡原则,才能保持晶体结构稳定。而对异价类质同象替换时,电荷平衡就起主导作用,而离子的半径差别则退居次要地位,因此半径差别的限制比较松散、不严格。
(3)离子类型与化学键。在发生类质同象替换中不改变晶体的键性。而离子或原子在形成晶格时的键性与其最外层电子构型有关,一般惰性气体型离子形成化合物时以离子键结合;而铜型离子形成化合物时以共价键、金属键结合。在晶格中这两类离子是不能发生类质同象替换的。如Ca2+与Hg2+呈八面体配位时的半径很接近,仅差0.002nm,且电价相同。但由于二者离子类型不同,所以二者不发生类质同象替换。
(4)晶格能。质点由自由状态结合成晶体时所释放出来的能量。而一个离子从自由状态进入晶格时释放出的能量被称为该离子的能量系数。在其他条件相似的情况下,能量系数大的离子替换能量系数小的离子时,则有利于降低晶格能,导致类质同象现象容易发生;反之,由能量系数小的离子替换能量系数大的离子时,则使晶格内能升高,导致原有晶格破坏,使类质同象现象不容易发生。
离子的能量系数与离子的电价的平方成正比,与离子半径成反比。即在离子半径相似情况下,高价离子的能量系数比低价离子的大,所以在元素周期表从左上方到右下方的对角线方向中,一般右下方的高价离子在晶格中容易替换左上方的低价离子形成“离子替换对角线”法则。见表6-6。
表6-6 异价类质同象代替的对角线法则(据潘兆橹,1993)
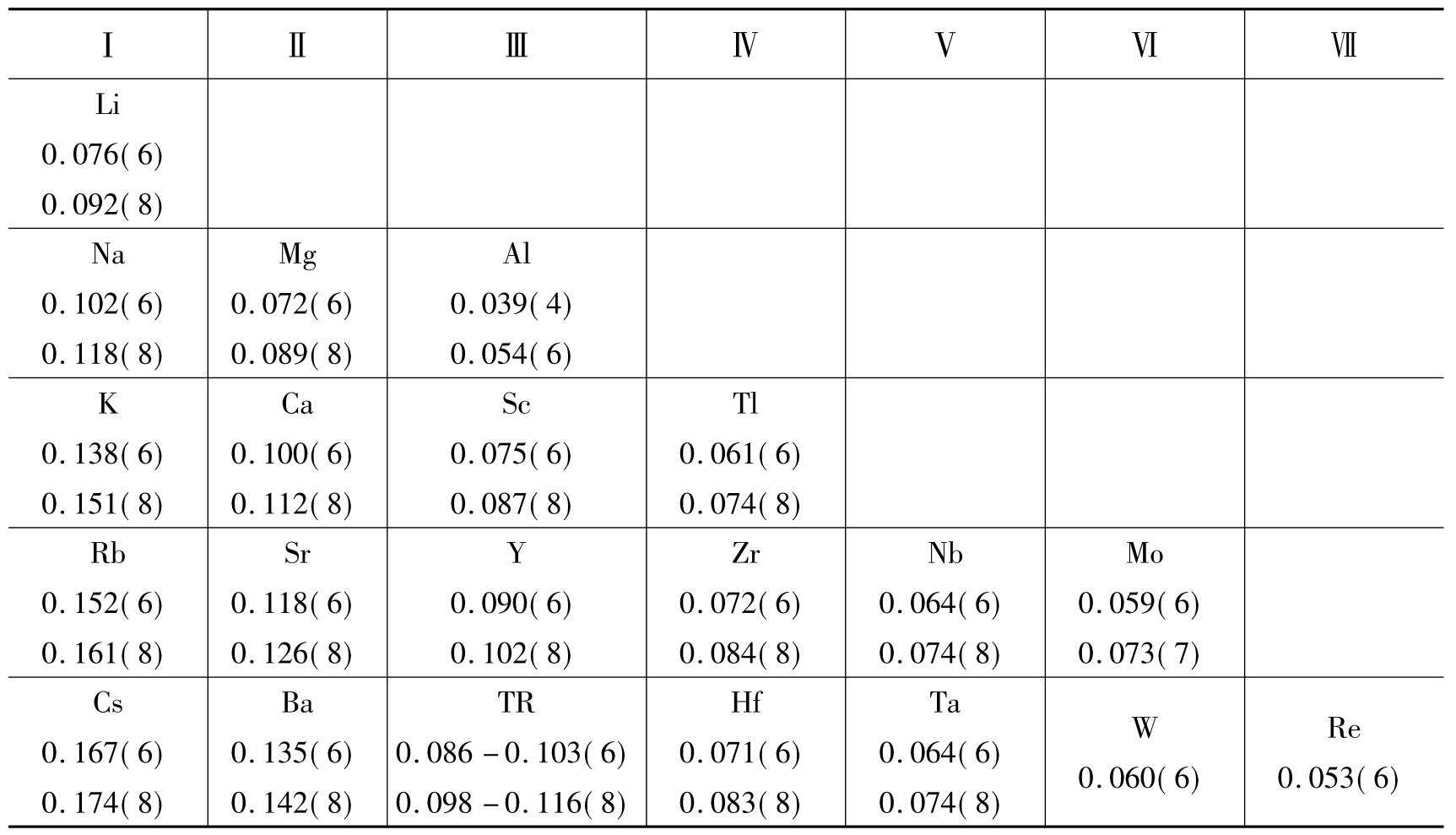
说明:表中的数据为离子有效半径,单位为nm,括号中数字为配位数。离子的正电价与所处的族数相同。
2.外部条件
外部条件,又称发生类质同象的外因条件。这些外部形成的环境条件主要有:
(1)温度。一般情况下,温度的升高有利于类质同象的发生;而温度下降则不利于类质同象形成,甚至促使已形成的类质同象晶体发生离熔现象。如高温形成的碱性长石晶体中,Na、K可以呈类质同象替换进入晶格,随着温度的下降,Na、K产生离熔,分别形成钠长石和钾长石晶体而组成条纹长石。
(2)压力。一般情况下,压力增大则不利于类质同象发生,甚至促使已形成的类质同象晶体发生离熔现象。
(3)组分浓度。一种晶体形成时,当介质中各种组分不能与晶体成分量比相适应时,即某种组分含量不足,则会由介质中存在的与这一组分性质相似的组分以类质同象替换的形式进入晶格加以补偿。例如磷灰石Ca5[PO4]3(F、Cl、OH)在岩浆中结晶时,由于环境中Ca2+数量不足,其不足部分则由介质中与Ca2+相似的Ce3+以类质同象替换Ca2+的方式进入晶格,这被称为补偿类质同象替换。
(4)在自然界中,一些微量元素由于含量不足或元素行为等因素难以形成独立矿物,常以类质同象的形式进入与其性质相似的一些常量元素所形成的晶格中,如辉钼矿中的Re。
(四)研究类质同象现象的意义
由于类质同象现象是自然界矿物晶体中最常见的一种结晶现象,它也是引起矿物化学成分变化的一个重要原因。对它的研究不仅理论上具有重要意义,而且也有着重要的实际应用价值。
地壳中的分散元素、稀有元素大部分无法形成独立的矿物,主要以类质同象替换的方式存在于和它性质相似的常量元素所形成的矿物晶格中,如Cd、In等存在于闪锌矿晶格中,Re存在于辉钼矿晶格中,Hf存在于锆石中等。研究这些元素类质同象替换规律,对于某些矿产资源的寻找和综合合理利用有着极为重要的意义。
元素间类质同象的替换会引起矿物晶体化学成分有规律的变化,也会导致其物理性质、化学性质产生有规律的改变,也是外界形成环境条件的表现。所以系统研究这些变化规律可以鉴定矿物,确定矿物化学组成,探索矿物形成的规律及研究矿物所属地质体的成因均具有重要的意义。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。















