第二节 水和无机盐
一、水及其特征
生命起源于水,水是生命不可缺少的物质。水在生物体内含量丰富,例如人体内水分约占人体体重的60%,腔肠动物体内水分高达90%。一般来说,水生生物和幼年的动、植物含水量较多,柔软的组织和器官含水量远远高于其他部分。例如人体大脑中水分占70%,眼球玻璃体的含水量达99%,坚硬的骨骼只含水20%~25%。
1.水分子结构特征
常温常压下水是无色、无味、无嗅的透明液体,水分子由一个氧原子和两个氢原子以共价键形成“V”形结构。氧原子有6个最外层电子,其中两个电子分别与两个氢原子的外层电子配对形成两个共价键,此共价键为极性键,因此水分子电荷呈非对称分布,是极性分子。除了同一水分子中的氢、氧原子间能形成共价键外,不同水分子之间的氢、氧原子间还能形成氢键。每一个水分子都能与其他四个水分子通过氢键连接成正四面体的排列形式(图2-4),因此整个水体的分子排列是比较规则的。
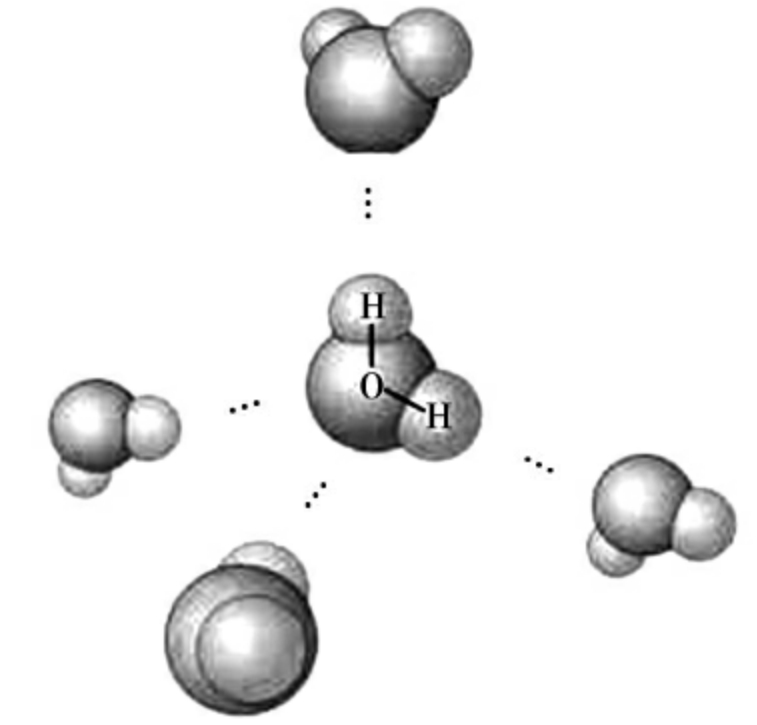
图2-4 水分子间形成的氢键
大球为O原子,小球为H原子,两者之间形成极性共价键。每个水分子可以和4个相邻的水分子形成氢键,用虚线表示,呈正四面体排列。
2.水的特性
水的特性是由水分子的极性以及易形成氢键的特点所决定的。由于极性和氢键作用,水分子聚集并规则地排列在一起,使得水在汽化时所需的热量很高,破坏氢键所消耗的能量也很高。所以,水的比热、汽化热和沸点都很高。比热是指使1g物质温度提高1℃所需要的热量。水的比热比任何液体和固体都大,因此水的温度不会因为吸收大量的热而发生明显波动。这对恒温动物体温的维持有重大意义。汽化热是指1g物质由液体转变为气体所需要的热量。水在汽化时可以带走大量的热,例如植物叶片的蒸腾作用及动物出汗,都可使有机体降温。水是良好的溶剂。由于水的极性,使水能很容易地溶解其他极性分子,例如生物体体液、血液中溶解的蛋白质、葡萄糖等。电解质类物质也很容易溶于水中。例如氯化钠结晶在水中,其表面的钠离子和氯离子与水接触,与水分子产生电亲和性,水分子中的氧原子带有负电荷与钠离子粘着,氢原子带有正电荷,与氯离子粘着,水分子将钠离子与氯离子分开,而使氯化钠溶于水中。水不仅是溶剂,本身也是生命过程中某些化学反应的反应物或产物。由于氢键的存在,使水在常温和体温下远未达到沸点,由此保证了生物体中的化学反应能正常进行。氢键使水分子之间形成的强内聚力使水体表面的张力增强。例如加满水的杯子,液面高于杯口却能长时间保持不溢出;一些水生生物可以停留在水面上或在水面上行走等。水的极性使水分子与其他分子表面带电荷的物质之间具有较强的吸附力。内聚力和吸附力形成水的毛细作用。温度降低,水分子运动减慢,有利于分子间氢键的形成。在4℃时,水的比重最大,沉在下面。低于4℃以后,水分子逐渐形成很开放的晶体结构,即每个水分子都以氢键与另外四个水分子相结合(图2-5),体积增大,密度降低,漂在水面。所以结冰总是从水面开始,冰层以下还是液体状态,温度也会高于表面,这为水生动物过冬提供了很好的条件。
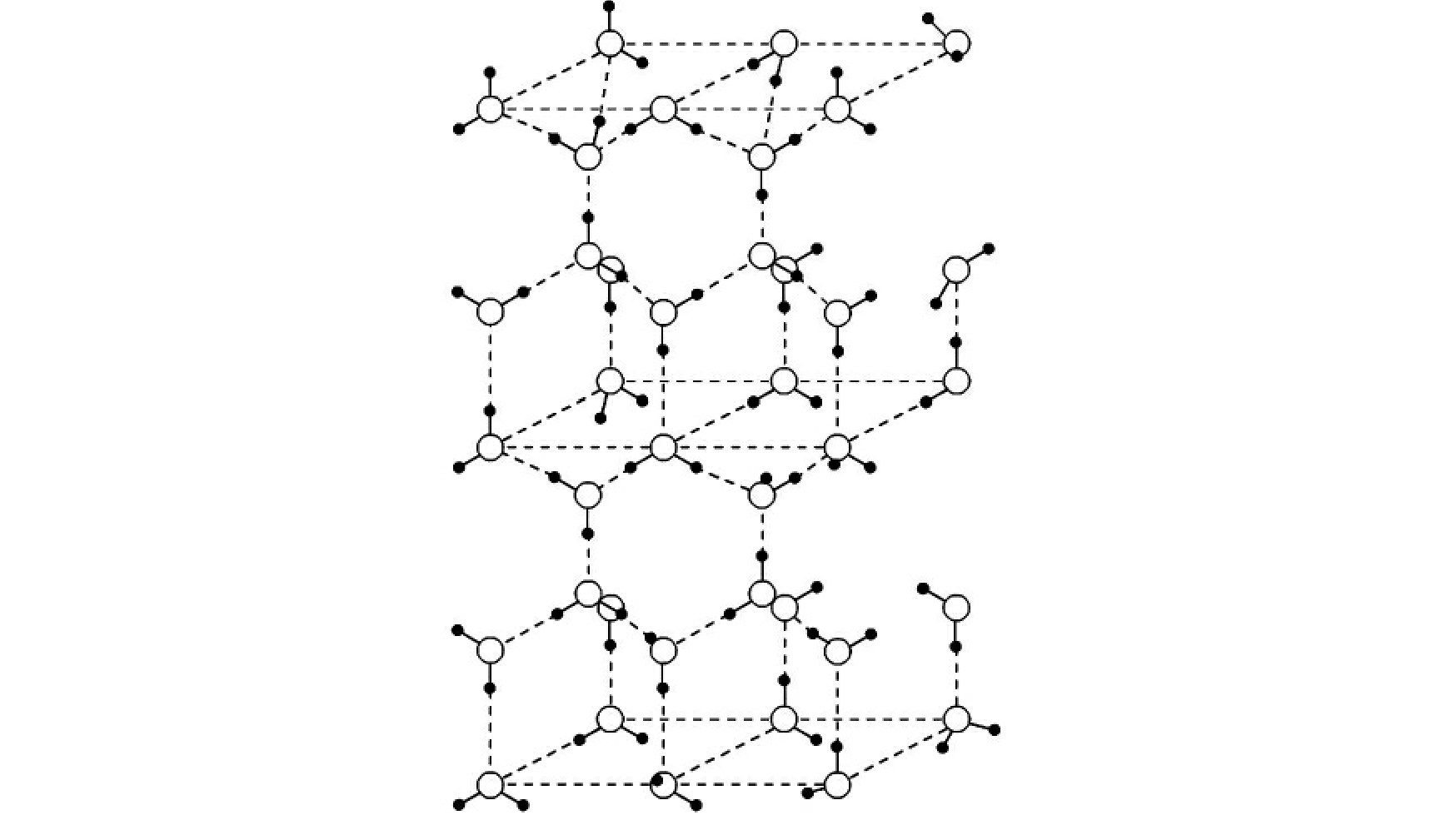
图2-5
水形成冰后,氢键将水分子固定成固态。由虚线构成的平行四边形代表一个平面。
二、无机盐
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。

















