第2章 金属和合金的结构与结晶
不同类别的金属材料其性能各有差异,即使是同种金属材料,在不同的加工工艺条件下,其力学性能也可能有较大差异。这种性能差异是由金属的内部微观结构所决定的。因此,了解金属的内部微观结构及其对金属性能的影响,将对选择材料及其加工工艺,具有非常重要的意义。
2.1 金属的晶体结构
金属和合金在固态下通常都是晶体,它们的很多特性与其结晶状态有关。要了解金属与合金的内部微观结构,首先要掌握其晶体结构的情况。
2.1.1 晶体的基本概念
固体物质按原子聚集状态不同分为晶体与非晶体两大类。晶体的原子按一定几何形状作有规律排列,如金刚石、石墨及一切固态的金属和合金,如图1.2.1(a)所示。而非晶体内部原子是无规则堆积在一起的,如玻璃、沥青、松香等。由于晶体和非晶体的内部结构不同,两者的性能也不同:晶体具有固定的熔点和各向异性的特征,而非晶体则没有固定的熔点,并且是各向同性。
通过X线晶体结构分析,可以测得晶体中原子的排列规律,如图1.2.1(a)所示。为了便于描述晶体内部原子排列的规律,将每一个原子抽象成一个几何点,把这些几何点用直线连接起来,使之构成一个空间格子,如图1.2.1(b)所示。这种描述原子在晶体中规律排列方式的空间格子称为晶格。
晶格实质上是由一些最基本的几何单元重复堆砌而成的。因此只要取晶格中的一个最基本的几何单元进行分析,便能从中找出整个晶格排列规律,如图1.2.1(c)所示。这种构成晶格的最基本的几何单元称为晶胞。
晶胞的大小以其各边尺寸a,b,c表示,称为晶格常数,度量单位均为Å(1Å= 1×10-10 m)。晶胞各边之间的夹角分别以α,β,γ表示,如图1.2.1(c)所示。
各种晶体由于其晶格类型和晶格常数不同,则呈现出不同的物理、化学及力学性能。
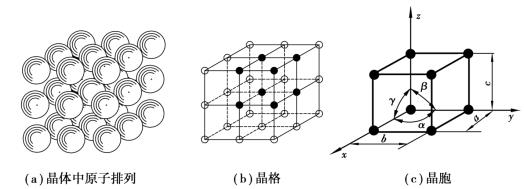
图1.2.1 简单立方晶格与晶胞示意图
2.1.2 常见的金属晶格类型
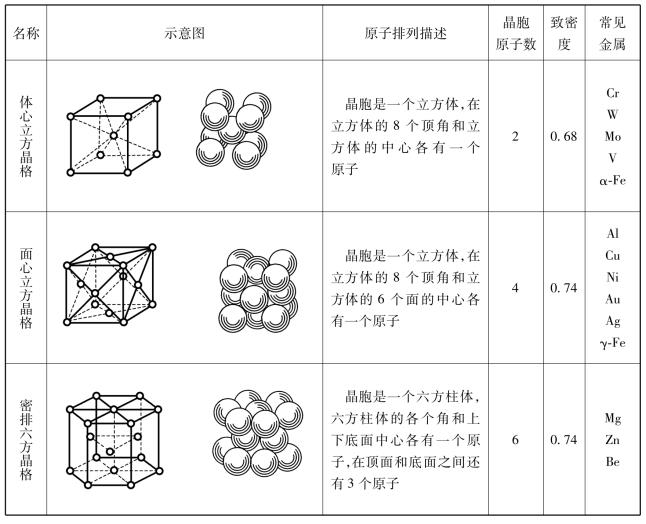
金属晶格类型常见的有3种:体心立方晶格、面心立方晶格、密排六方晶格,见表1.2.1。金属晶格类型不同,其原子排列的紧密程度(致密度)不同。面心立方和密排六方晶格的原子密度大,体心立方晶格的原子密度稍小。因此,金属晶格类型的改变将引起金属体积和性能的变化。
表1.2.1 常见的金属晶格类型
2.1.3 金属的实际晶体结构
(1)多晶体结构
结晶方位完全一致的晶体称为“单晶体”。单晶体具有各向异性的特征,即在晶体的各个晶向上具有不同的物理、化学和力学性能。实际使用的金属不是单晶体而是多晶体,并且存在着各种晶体缺陷。
将实际使用的金属材料制成试样,在显微镜下观察,可以看到它是由许多小晶体组成的,这种外形不规则的小晶体称为晶粒,晶粒与晶粒之间的界面称为晶界。多晶体中,虽然每个晶粒和单晶体一样具有各向异性,但一块金属包含有大量彼此位向不同的晶粒,不同方向的金属性能都是许多晶粒性能的平均值,故一般金属具有各向同性特征。实际金属的显微组织照片和多晶体结构示意图如图1.2.2所示。
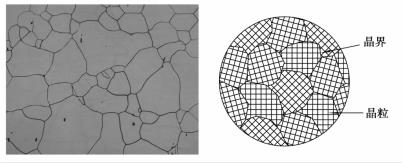
图1.2.2 多晶体的晶粒和晶界示意图
(2)晶体缺陷
在金属晶体中,由于晶体形成条件、原子热运动及其他各种因素的影响,原子规则排列受到破坏,呈现出不完整,通常把这种区域称为晶体缺陷。根据晶体缺陷的几何特征,可分为点缺陷、线缺陷和面缺陷3类。
1)点缺陷
最常见的点缺陷有晶格空位、置换原子和间隙原子,如图1.2.3所示。由于点缺陷的出现使周围的原子出现“撑开”或“靠拢”的现象,这种现象称为晶格畸变。晶格畸变的存在,使金属产生内应力。晶体性能发生变化,如强度、硬度和电阻增加,体积发生变化,它也是强化金属的手段之一。
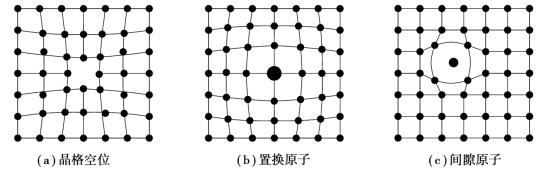
图1.2.3 点缺陷示意图
2)线缺陷
线缺陷主要是指位错。位错的形式很多,其中最常见的一种形式是刃型位错,如图1.2.4所示。刃型位错的表现形式是在晶体的某一晶面上,多出一排原子面,它好像一把刀刃插入晶体中,使该晶面上、下两部分晶体间产生错排现象,故称为刃型位错。在位错线附近一定范围内,晶格发生了畸变。
位错的存在对金属的力学性能有很大的影响,例如,当金属材料处于退火状态时,位错密度较小,强度最低;若金属材料经过冷变形加工后,位错密度增大,提高了金属的强度。
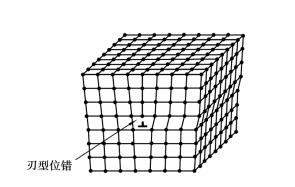
图1.2.4 晶体中刃型位错示意图
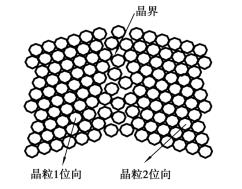
图1.2.5 晶界的过渡层结构示意图
3)面缺陷
面缺陷通常是指晶界。实际金属材料都是多晶体结构,在多晶体中两个相邻晶粒之间的晶格位向是不同的,所以晶界处的原子的排列是不规则的,它是从一种位向逐渐过渡到另一种位向的过渡层,如图1.2.5所示。由于晶界处的原子排列不规则,使晶格处于畸变的状态,因而在常温下晶界对金属的塑性变形起阻碍作用,即晶界处有较高的硬度和强度。当晶粒越细小时,晶界的面积越多,对金属塑性变形的阻碍越大,金属的强度和硬度也越高。此外,晶界处原子扩散速度较快,熔点低和容易被腐蚀等。
2.2 金属的结晶过程和同素异构转变
金属的性能与其组织有关,而组织与结晶过程有关,因而要了解金属的结晶规律,以便控制结晶过程,形成希望得到的组织和性能。
2.2.1 纯金属的结晶
(1)结晶的概念
除少数粉末冶金制品外,绝大多数金属制件都是经过熔化、冶炼和浇注而获得的,这种由液态转变为固态的过程称为凝固。如果凝固的固态物质是晶体,则这种凝固又称为结晶。一般金属固态下都是晶体,因而金属凝固过程可称为结晶。
(2)纯金属的冷却曲线
纯金属都有一个固定的熔点(或结晶温度),高于此温度熔化,低于此温度才能结晶成为晶体。金属的结晶温度通常用热分析等实验方法来测定。图1.2.6所示为纯金属的冷却曲线,其原理是在液态金属的缓慢冷却的过程中,每隔一定时间测量一次温度,直到冷却至室温。然后将测量的结果绘制在温度-时间的坐标上,就可得到纯金属的冷却曲线。
由冷却曲线可见,液态金属随时间的延长,它所含的热量不断散失,其温度也不断下降,但当冷却到某一温度时,冷却的时间虽然增加,但温度并不下降,在冷却曲线上出现了一个水平线段,这个水平线段所对应的温度就是纯金属进行结晶的温度。出现水平线段的原因,是由于结晶时放出的结晶潜热补偿了金属向外界散失的热量。结晶完成后,由于金属继续向周围环境散热,故温度又重新下降。
纯金属在极其缓慢的冷却条件下测得的结晶温度称为理论结晶温度T o。但在实际生产中,金属由液态结晶为固态都有较大的冷却速度,此时金属要在理论结晶温度以下某一温度才开始进行结晶,这一温度称为实际结晶温度T n。金属的实际结晶温度低于理论结晶温度的现象称为过冷现象。而理论结晶温度与实际结晶温度之差称为过冷度,用ΔT表示,即ΔT= T n- T o。金属结晶时的过冷度大小与冷却速度有关,冷却速度越大,过冷度就越大,即金属的实际结晶温度越低。
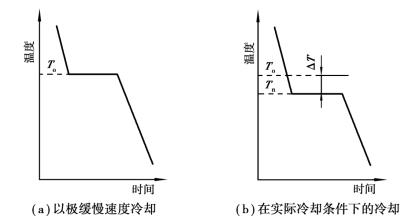
图1.2.6 纯金属结晶时的冷却曲线
2.2.2 纯金属的结晶过程
金属结晶时,首先从液态金属中形成一些极细小的晶体,这些极细小的晶体称为晶核,它不断吸附周围液体中的原子而长大。与此同时,在液体中又不断产生新的晶核并相继长大,直到全部液体凝固为止,最后金属便由许多外形不规则的小晶体(晶粒)所组成,如图1.2.7所示。因此,液体金属的结晶过程包括晶核的形成和晶核的长大两个基本过程,而且这两个过程是同时进行的。
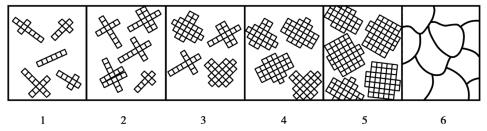
图1.2.7 纯金属结晶过程示意图
(1)晶核的形成
当液态金属冷至结晶温度以下时,某些近似晶体原子排列的小原子集团便成为结晶核心,这种由液态金属内部自发形成结晶核心的过程称为自发形核。但在实际金属中常有杂质存在,这些杂质固态质点的存在能够促进在其表面上形成晶核。这种依附于杂质而形成的晶核称为非自发形核。自发形核和非自发形核在金属结晶时同时进行的,但非自发形核比自发形核更为重要,在金属结晶过程中起优先和主导作用。
(2)晶核的长大
晶核形成后,当过冷度较大或金属液体中存在杂质时,金属晶体常以树枝状的形式生长,在晶核开始长大初期,因其内部原子规则排列的特点,故外形也是比较规则的。但随着晶核的继续长大,形成了晶体的尖角和棱边,由于尖角和棱边处的散热条件优于其他部位,并易于存在晶体缺陷等原因,晶体在顶角和棱边处优先长大,其生长方式像树枝一样,先长出干枝,称为一次晶轴,然后在一次晶轴伸长和变粗的同时,在其侧面棱角和缺陷处又长出分枝,称为二次晶轴。随着时间的延长,二次晶轴长成的同时又长出三次晶轴等,如此不断成长和分枝下去,直至液体全部消失,最后得到的晶体称为树枝状晶体(简称枝晶),每一枝晶将成长为一个晶粒。
2.2.3 金属结晶后晶粒的大小
晶粒大小对金属力学性能的影响
金属结晶后是由许多晶粒组成的多晶体。晶粒的大小对金属的力学性能有很大的影响。一般情况下,晶粒越细小,金属的强度、塑性和韧性越好。为了提高金属的力学性能,希望得到细晶组织,因此必须了解影响晶粒大小的因素及其控制方法。
结晶后的晶粒大小主要取决于形核率N(单位时间、单位体积内所形成的晶核数目)与晶核的长大速率G(单位时间内晶核向周围长大的平均线速度)。显然,凡能促进形核率N,抑制长大速率G的因素,均能细化晶粒。
在生产中,为了获得细晶粒组织,常采用以下方法:
1)增加过冷度
形核率和长大速率都随过冷度增大而增大,但在很大的范围内形核率比晶核长大速率增长得更快。故过冷度越大,单位体积中的晶粒数目越多,晶粒越细小。这种生产方法适用于中、小型铸件的生产。
2)变质处理
对于一些大型铸件,由于散热较慢,要获得较大的过冷度很困难,且较大的过冷度往往导致铸件开裂而造成废品。为了获得细晶粒组织,通常在浇注前向液态金属中人为地加入一些细小的变质剂,使其大量增加非自发晶核,从而得到细晶粒组织。这种细化晶粒的方法称为变质处理。例如,向钢液中加入铝、钒、硼;向铸铁中加入Si-Fe;向铝液中加入钛、锆等。变质处理在生产中应用广泛。
3)振动
机械振动、超声波振动、电磁振动使枝晶折断、破碎,也能使晶核数目增多,从而细化晶粒。
2.2.4 金属的同素异构转变
金属在固态下,由一种晶格转变为另一种晶格的过程称为同素异构转变。如铁、钛、锰、锡等均有同素异构转变的性能。纯铁的同素异构转变过程如图1.2.8所示,从图中可以看出,纯铁在1 538℃时开始结晶,在1 538~1 394℃时为体心立方晶格,称为δ-Fe;温度下降到1 394~912℃时为面心立方晶格,称为γ-Fe;在912℃以下为体心立方晶格,称为α-Fe。纯铁的同素异构转变过程可概括如下:
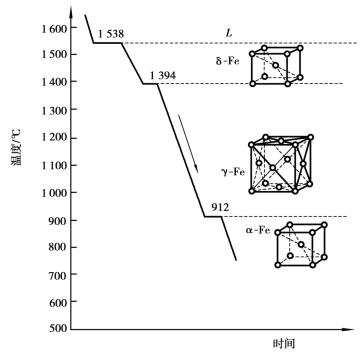
图1.2.8 铁的同素异构转变
![]()
金属的同素异构转变也是通过原子的重新排列来完成的,它与液态金属结晶过程很相似,也包括晶核的形成和晶粒的长大两个阶段,为了便于两者的区别,一般将固态同素异构转变称为二次结晶或重结晶,液态金属结晶称为一次结晶。由于在固态下原子的扩散比液态下困难得多,因此同素异构转变应具有较大的过冷度。此外,由于晶格类型不同,其原子排列的致密度不同,将会使金属的体积发生变化并产生较大的内应力。
由于纯铁具有同素异构转变的特性,因此它是钢铁能够进行热处理的依据,也是钢铁材料性能多种多样、用途广泛的主要原因之一。
2.3 合金的晶体结构
纯金属虽具有较好的导电性、导热性和良好的塑性等优点,但由于其力学性能的强度、硬度较低,不能满足工业上使用性能的要求,且冶炼困难、价格较高,因此应用较少。一般机械工业中广泛使用的金属材料是合金,其中铁碳合金(钢铁)就是使用最为广泛的一种。
2.3.1 合金的基本概念
(1)合金
一种金属元素与其他金属元素或非金属元素,经熔炼、烧结或其他方法结合成具有金属特性的物质称为合金,如碳钢是铁和碳组成的合金;黄铜是铜和锌组成的合金。
(2)组元
组成材料的最基本、能独立存在的物质称为组元(简称元)。一般来说,组元是组成该材料的元素,但稳定的化合物也可以作为组元。例如,黄铜的组元是铜和锌,青铜的组元是铜和锡,而在铁碳相图中的组元则是铁和稳定化合物Fe3 C。由两个组元组成的合金称为二元合金,三个组元组成的合金称为三元合金。
(3)合金系
由给定的组元可以以不同的比例制成一系列成分不同的合金,这一系列合金就构成一个合金系。例如,凡是由铜和锌组成的合金,不论其成分如何,都属于铜锌二元合金系,或称铜锌合金;铁和碳组成的合金称为铁碳二元合金系,也称铁碳合金。
(4)相
合金中具有同一聚集状态、同一结构和性质的均匀组成部分称为相。例如,水为液态物质称为液相;冰为固态物质称为固相;同样是固态物质,有时物质是单相的,而有时是多相的,如珠光体是由铁素体和渗碳体两相组成。
(5)组织
由单相或多相组成具有独特微观形貌特征的部分称为组织。组织反映材料的相组成、相形态、大小和分布状况,因此组织是决定材料最终性能的关键。在研究合金时通常用金相法对组织加以鉴别。
2.3.2 合金组织
合金在液态下,各组元相互溶解,只有一种液相。在固态下合金中的相可分为固溶体和金属化合物两大基本类型,由于各组元相互作用不同,合金的相结构可分固溶体、金属化合物和机械混合物3种形式。
(1)固溶体
某种元素的晶格中溶入其他元素原子组成的相称为固溶体。形成固溶体后,晶格保持不变的组元称为溶剂;晶格消失或被溶解的组元称为溶质。由此可知,固溶体的晶格类型与溶剂组元相同,显微形貌也与溶剂相同。
固溶体的浓度通常是指固溶体中溶质所占的质量百分数。在一定条件下,溶质元素在固溶体中的极限浓度称为固溶体的溶解度。凡溶解度有一定限制的固溶体称为有限固溶体,若两个组元可以以任意比例相互溶解,则称为无限固溶体。
根据溶质原子在溶剂晶格分布情况不同,固溶体可分为置换固溶体和间隙固溶体两种。
1)置换固溶体
溶剂晶格结点上的部分原子被溶质原子所替代而形成的固溶体,称为置换固溶体,如图1.2.9(a)所示。一般情况是当溶质原子与溶剂原子直径差别不大时,易于形成置换固溶体。通常两组元原子半径差别较小,晶格类型相同,原子结构相似,固溶体溶解度大,可以形成无限固溶体,如铜和镍组成的合金,在固态下形成α无限固溶体。
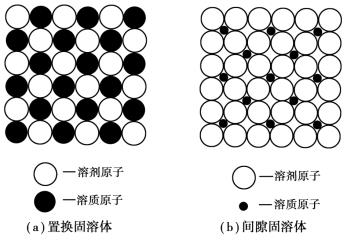
图1.2.9 固溶体的两种类型
当两组元原子半径差别较大,往往只能形成有限固溶体。实际上,大多数合金都是有限固溶体,并且溶解度随温度升高而增大。
2)间隙固溶体
溶质原子溶入溶剂晶格空隙处而形成的固溶体称为间隙固溶体,如图1.2.9(b)所示。一般情况是只有溶质原子直径与溶剂原子直径之比小于0.59时,才能形成间隙固溶体。例如,原子直径很小的非金属元素C,N,H,B为溶质,溶入过渡族金属中形成的均为间隙固溶体。间隙固溶体的溶解度都是有限的。
3)固溶体的力学性能
无论是置换固溶体还是间隙固溶体,溶质原子的溶入,都会使晶格发生畸变,同时晶体的晶格常数也要发生变化,原子尺寸相差越大,畸变也越大,使塑性变形阻力增加,从而提高了合金的强度和硬度,而塑性下降,这种现象称为固溶强化。固溶强化是提高金属材料力学性能的重要途径之一。
(2)金属化合物
合金中溶质含量超过溶剂的溶解度后,会出现新相。这个新相可能是另一种固溶体,也可能是晶格类型和性能完全不同于任一组元的新相,称为化合物。一般可用化学分子式表示,如Fe3 C,TiC,CuZn等。
金属化合物一般具有熔点高、硬度高、脆性大的特点,在合金中主要作为强化相,如Fe3 C在钢中存在,将使钢的强度、硬度、耐磨性提高,但使钢的塑性和韧性下降。因此,利用改变金属化合物的数量、形状、大小和分布来提高金属材料的力学性能,也是强化金属材料的重要途径之一。
由于化合物的结合键及晶格类型的多样性,使它具有许多特殊的物理化学性能,其中已有不少正在开发应用,作为新的功能材料和耐热材料,对现代科学技术的进步起着重要的推动作用。例如具有半导体性能的砷化镓(GaAs),其性能已远远超过正在广泛应用的硅半导体材料,目前正应用在发光二极管的制造上,作为超高速电子计算机的元件已引起了世界的关注。此外,还有记忆合金NiTi和CuZn、核反应堆材料Zr3 Al以及作为新一代能源的储氢材料LaNi5等。
(3)机械混合物
固溶体、金属化合物是组成合金的基本相。由两种或两种以上的相按一定质量百分数组合而成的物质称为机械混合物。例如,铁素体和渗碳体在某种条件下形成的机械混合物称为珠光体。机械混合物的性能取决于各组成相的性能,以及各相的数量、形状、大小和分布。
2.4 二元合金相图
合金相图是用来表示合金系的平衡相与成分、温度之间关系的图形,又称合金状态图或合金平衡相图。应用合金相图,可清晰了解合金在缓慢加热或冷却过程中的组织转变规律。所以,相图是进行金相组织分析、制订铸造、锻压、焊接、热处理热加工工艺的重要依据。
2.4.1 二元合金相图的建立
相图都是通过实验方法建立起来的,最常用的是热分析法。现以Cu-Ni合金为例,说明用热分析法测绘二元合金相图的基本步骤。
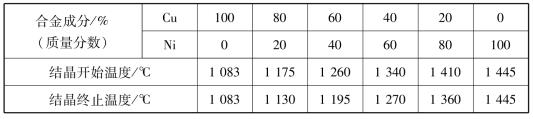
①配制不同成分的Cu-Ni合金,见表1.2.2。
表1.2.2 不同成分的Cu-Ni合金
②用热分析法分别测出各组合金的冷却曲线(缓慢冷却),并找出各冷却曲线上的临界点的温度。
③画出温度-成分坐标系,在各合金成分的垂线上标出临界点温度。
④将物理意义相同的临界点连接起来,即获得Cu-Ni合金相图,如图1.2.10所示。
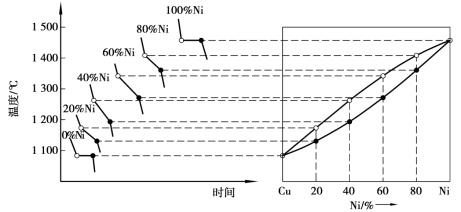
图1.2.10 Cu-Ni合金的冷却曲线及相图
2.4.2 二元合金相图的分析
(1)匀晶相图
两组元在液态下和固态下均能无限互溶所构成的相图称为二元匀晶相图。属于该类相图的合金有Cu-Ni,Fe-Cr,Au-Ag等。下面以Cu-Ni合金为例,对二元匀晶相图进行分析。
1)相图分析
图1.2.11为Cu-Ni合金相图。图中A点(1 083℃)是纯铜的熔点,B点(1 452℃)是纯镍的熔点。上面一条曲线为液相线,该线以上区域的合金全部为液相的单相区。任何成分的合金从液态冷却到液相线时,就开始结晶出固体。下面一条曲线为固相线,在该线以下区域合金全部转变为固相,也是单相区。在液相线和固相线之间的区域是液相和固相共存的两相区。因此,匀晶相图是由两条曲线,分隔开两个单相区和一个两相区组成。
2)合金的结晶过程
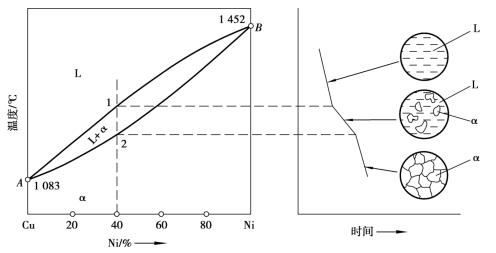
图1.2.11 Cu-Ni匀晶相图
以w Ni= 40%的合金为例说明Cu-Ni合金的结晶过程。由图可见,其成分垂线与液相、固相分别相交于1和2两点,当合金以极缓慢速度冷却到1点时,开始从液相中结晶出α固相,随着温度的不断降低,α固相不断增多,而剩余的L相不断减少,并且液相和固相的成分通过原子扩散而分别沿着液相线和固相线变化。当温度下降到2点时,合金结晶终了,获得与原合金成分一致的α相固溶体。但在实际生产条件下,由于冷却速度较快,原子扩散来不及充分进行,导致先后结晶出来的固相成分存在差异,这种晶粒内部化学成分不均匀的现象称为晶内偏析,又称枝晶偏析。
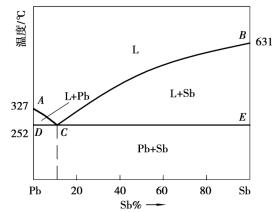
图1.2.12 Pb-Sb共晶相图
(2)共晶相图
两组元在液态无限互溶,在固态下有限溶解,通过共晶反应形成两相机械混合物的二元相图称为二元共晶相图。具有这类相图的合金有Pb-Sn,Pb-Sb,Cu-Ag等。下面以Pb-Sb合金为例进行分析:
1)相图分析
如图1.2.12所示,在Pb-Sb合金相图中,A点为纯Pb的熔点,B点为纯Sb的熔点,ACB线为液相线,即在此线以上的Pb-Sb合金都是液相。而DCE线为固相线,在低于固相线温度时,各种成分的Pb-Sb合金都是固相。在ACB和DCE两线之间是液、固两相共存的两相区。
2)合金的结晶过程
图1.2.13为共晶合金的结晶示意图。当成分为11% Sb和89% Pb的合金,在结晶前即不形成Sb,也不形成Pb,冷却到C点时,开始结晶,并同时从液态合金中结晶出Pb和Sb的共晶体。这种从一种液态中同时结晶出两个固相的过程称为共晶转变(也称共晶反应),即Lc→(Pb+Sb),因此,固相线DCE线也称共晶线,C点称为共晶点。C点以下合金不再发生变化,最终组织为(Pb+ Sb)的共晶体。
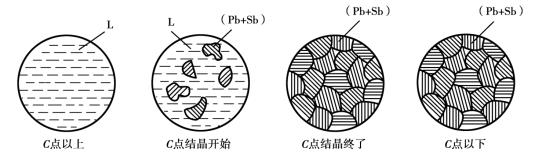
图1.2.13 共晶合金的结晶示意图
含Sb量低于11%的合金,其结晶后的产物为Pb+(Pb+ Sb)的组织,称为亚共晶组织;含Sb量高于11%的合金,结晶后的产物为Sb+(Pb+ Sb)的组织,称为过共晶组织。
免责声明:以上内容源自网络,版权归原作者所有,如有侵犯您的原创版权请告知,我们将尽快删除相关内容。

















